
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
 Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH__________ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©
Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH__________ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©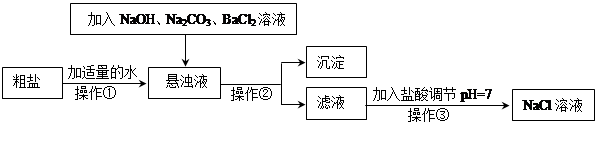 ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ| AΘ°œ»Φ”»κNaOHΘ§ΚσΦ”»κNa2CO3Θ§‘ΌΦ”»κBaCl2»ή“Κ |
| BΘ°œ»Φ”»κNaOHΘ§ΚσΦ”»κBaCl2»ή“ΚΘ§‘ΌΦ”»κNa2CO3 |
| CΘ°œ»Φ”»κBaCl2»ή“ΚΘ§ΚσΦ”»κNaOHΘ§‘ΌΦ”»κNa2CO3 |
| DΘ°œ»Φ”»κBaCl2»ή“ΚΘ§ΚσΦ”»κNa2CO3Θ§‘ΌΦ”»κNaOH |
 Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©
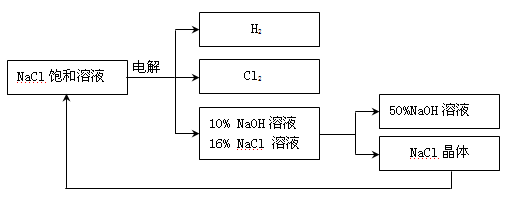
Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©Θ®10Ζ÷Θ©“‘ΒγΫβ ≥―ΈΥ°ΈΣΜυ¥Γ÷Τ»Γ¬»ΤχΓΔ«β―θΜ·ΡΤΒ»≤ζΤΖΒΡΙΛ“Β≥ΤΈΣΓΑ¬»ΦνΙΛ“ΒΓ±Θ§Υϋ «ΡΩ«ΑΜ·―ßΙΛ“ΒΒΡ÷Ί“Σ÷ß÷υ÷°“ΜΓΘ
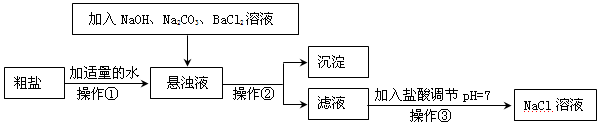
Δώ.”…”Ύ¥÷―Έ÷–Κ§”–…ΌΝΩMgCl2ΓΔCaCl2ΓΔNa2SO4Β»‘”÷ Θ§≤ΜΖϊΚœΒγΫβ“Σ«σΘ§“ρ¥Υ±Ί–κΨ≠ΙΐΨΪ÷ΤΓΘœ¬ΆΦ «¥÷―ΈΨΪ÷ΤΒΡΝς≥ΧΘΚ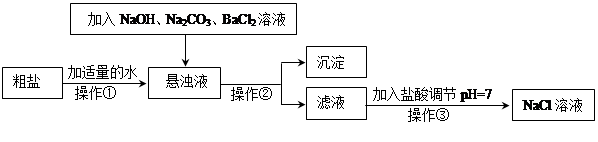 ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©≤ΌΉςΔΎΒΡΟϊ≥Τ « ΓΘ
Θ®2Θ©‘Ύ–ϋΉ«“Κ÷–Φ”NaOH»ή“ΚΓΔNa2CO3»ή“ΚΓΔBaCl2»ή“Κ»ΐ÷÷ ‘ΦΝΒΡΥ≥–ρΚœάμΒΡΈΣ ΓΘ
| AΘ°œ»Φ”»κNaOHΘ§ΚσΦ”»κNa2CO3Θ§‘ΌΦ”»κBaCl2»ή“Κ |
| BΘ°œ»Φ”»κNaOHΘ§ΚσΦ”»κBaCl2»ή“ΚΘ§‘ΌΦ”»κNa2CO3 |
| CΘ°œ»Φ”»κBaCl2»ή“ΚΘ§ΚσΦ”»κNaOHΘ§‘ΌΦ”»κNa2CO3 |
| DΘ°œ»Φ”»κBaCl2»ή“ΚΘ§ΚσΦ”»κNa2CO3Θ§‘ΌΦ”»κNaOH |
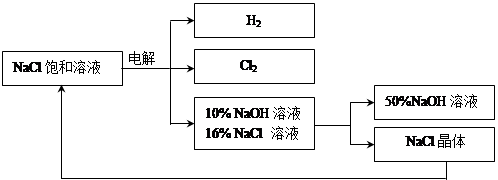
 Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©
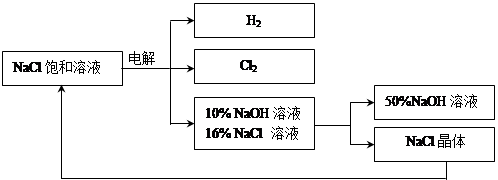
Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©Θ®10Ζ÷Θ©“‘ΒγΫβ ≥―ΈΥ°ΈΣΜυ¥Γ÷Τ»Γ¬»ΤχΓΔ«β―θΜ·ΡΤΒ»≤ζΤΖΒΡΙΛ“Β≥ΤΈΣΓΑ¬»ΦνΙΛ“ΒΓ±Θ§Υϋ «ΡΩ«ΑΜ·―ßΙΛ“ΒΒΡ÷Ί“Σ÷ß÷υ÷°“ΜΓΘ
Δώ.”…”Ύ¥÷―Έ÷–Κ§”–…ΌΝΩMgCl2ΓΔCaCl2ΓΔNa2SO4Β»‘”÷ Θ§≤ΜΖϊΚœΒγΫβ“Σ«σΘ§“ρ¥Υ±Ί–κΨ≠ΙΐΨΪ÷ΤΓΘœ¬ΆΦ «¥÷―ΈΨΪ÷ΤΒΡΝς≥ΧΘΚ
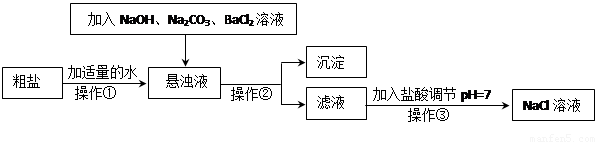 ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΜΊ¥πœ¬Ν–Έ ΧβΘΚ
Θ®1Θ©≤ΌΉςΔΎΒΡΟϊ≥Τ « ΓΘ
Θ®2Θ©‘Ύ–ϋΉ«“Κ÷–Φ”NaOH»ή“ΚΓΔNa2CO3»ή“ΚΓΔBaCl2»ή“Κ»ΐ÷÷ ‘ΦΝΒΡΥ≥–ρΚœάμΒΡΈΣ ΓΘ
AΘ°œ»Φ”»κNaOHΘ§ΚσΦ”»κNa2CO3Θ§‘ΌΦ”»κBaCl2»ή“Κ
BΘ°œ»Φ”»κNaOHΘ§ΚσΦ”»κBaCl2»ή“ΚΘ§‘ΌΦ”»κNa2CO3
CΘ°œ»Φ”»κBaCl2»ή“ΚΘ§ΚσΦ”»κNaOHΘ§‘ΌΦ”»κNa2CO3
DΘ°œ»Φ”»κBaCl2»ή“ΚΘ§ΚσΦ”»κNa2CO3Θ§‘ΌΦ”»κNaOH
”–Ά§―ßΧα≥ω”Ο »ή“Κ¥ζΧφBaCl2»ή“ΚΩ…¥οΒΫΆ§―υΒΡΡΩΒΡΓΘ
Δρ.œ¬ΆΦ «ΒγΫβ ≥―ΈΥ°÷Τ»Γ¬»ΤχΓΔ«β―θΜ·ΡΤΒ»≤ζΤΖΒΡΝς≥ΧΘΚ
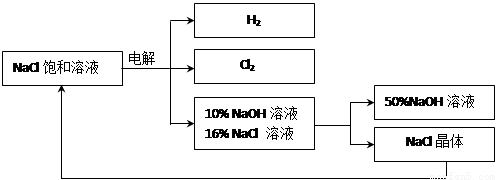
Θ®3Θ©‘ΎΒγΫβΙΐ≥Χ÷–Θ§ΖΔ…ζΒΡΖ¥”ΠΈΣ2NaCl + 2H2O Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH
ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©
Cl2 Γϋ+ H2 Γϋ + 2NaOHΘ§ΒγΫβΚσ»ή“ΚΒΡpH
ΓΘΘ®ΧνΓΑ…ΐΗΏΓ±ΓΔΓΑ≤Μ±δΓ±ΓΔΓΑΫΒΒΆΓ±Θ©
Θ®4Θ© ΒγΫβ ≥―ΈΥ° ±Θ§–ηΖά÷ΙCl2ΚΆNaOHΖ¥”ΠΘ§“ρCl2ΚΆNaOH»ή“Κ≥δΖ÷Ϋ”¥ΞΜα…ζ≥…NaClOΓΔ¬»Μ·ΡΤΓΔΥ°Θ§«κ–¥≥ωCl2ΚΆNaOH»ή“ΚΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ ΓΘ
Θ®5Θ©ΗΟΝς≥Χ÷–Ω…“‘―≠ΜΖάϊ”ΟΒΡΈο÷ « ΓΘ
Θ®6Θ©»τ»Γ100gΒΡ»ή÷ ÷ ΝΩΖ÷ ΐΈΣ25%ΒΡ¬»Μ·ΡΤ»ή“ΚΫχ––ΒγΫβΘ§“ΜΕΈ ±ΦδΚσΆΘ÷ΙΆ®ΒγΘ§…ζ≥…¬»ΤχΒΡ÷ ΝΩ7.1gΓΘ«κΦΤΥψΘΚ…ζ≥…«βΤχΒΡ÷ ΝΩΈΣΕύ…ΌΩΥΘΩΖ¥”ΠΚσ»ή“Κ÷–NaOHΒΡ÷ ΝΩΖ÷ ΐ «Εύ…ΌΘΩΘ®–¥≥ωΦΤΥψΙΐ≥ΧΘ§ΦΤΥψΫαΙϊΨΪ»ΖΒΫ0.1%Θ©
Θ®7Θ©»τ ΙΘ®6Θ©÷–ΒγΫβΚσΒΡ»ή“ΚΜ÷Η¥ΒΫ‘≠ά¥Ή¥Χ§Θ§‘ρ–ηœρ»ή“Κ÷–Φ”»κ ΝΩΒΡ ΓΘ
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com