
题目列表(包括答案和解析)
| 氯化钾 | 氯化钙 | 氯化钠 | 氯化镁 | 氯化铝 | 氯化锌 | ______ | 氯化铜 |
| KCl | CaCl2 | NaCl | MgCl2 | ______ | ZnCl2 | FeCl2 | CuCl2 |

 27、在金属活动性顺序中,活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来.张老师在做钠与硫酸铜溶液反应的演示实验时,观察到的现象是:钠块在液面上很快融成一个银白色小球,并四处游动,溶液中出现蓝色絮状沉淀,小球很快停在絮状沉淀集中处燃烧起来,并伴随有轻微的爆炸声,却始终没有发现在钠表面有红色固体析出.对此,同学们展开了如下探究:
27、在金属活动性顺序中,活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来.张老师在做钠与硫酸铜溶液反应的演示实验时,观察到的现象是:钠块在液面上很快融成一个银白色小球,并四处游动,溶液中出现蓝色絮状沉淀,小球很快停在絮状沉淀集中处燃烧起来,并伴随有轻微的爆炸声,却始终没有发现在钠表面有红色固体析出.对此,同学们展开了如下探究: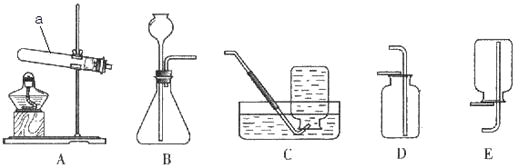
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com