
题目列表(包括答案和解析)
| 反应前 | 氧化铜被完全还原后 | 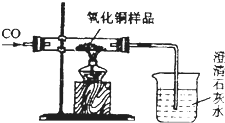 | |
| A组 | 玻璃管和氧化铜样品质量为m1g | 玻璃管和固体物质的质量为m2g | |
| B组 | 烧杯和澄清石灰水的质量为m3g | 烧杯和烧杯中物质的质量为m1g |
| 反应前 | 氧化铜完全反应后 | |
| 第一组 | 烧杯和澄清石灰水的总质量180.0g | 烧杯和烧杯内物质的总质量184.3g |
| 第二组 | 玻璃管和氧化铜样品的总质量是44.5g | 玻璃管和管内物质的总质量是42.9g |
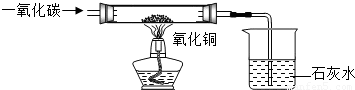
| 反应前 | 氧化铜完全反应后 | |
| 第一组 | 烧杯和澄清石灰水的总质量180.0g | 烧杯和烧杯内物质的总质量184.3g |
| 第二组 | 玻璃管和氧化铜样品的总质量是44.5g | 玻璃管和管内物质的总质量是42.9g |
| 反应前 | 氧化铜被完全还原后 | 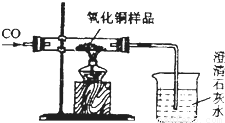 | |
| A组 | 玻璃管和氧化铜样品质量为m1g | 玻璃管和固体物质的质量为m2g | |
| B组 | 烧杯和澄清石灰水的质量为m3g | 烧杯和烧杯中物质的质量为m1g |
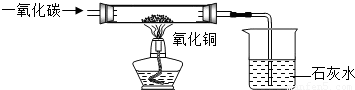
 (2005?西城区一模)现有含杂质的氧化铜样品(杂质不参加反应),为了测定该样品中氧化铜的质量分数,某同学称取12.5g样品,并用如图所示的装置进行实验,得到如下两组数据:
(2005?西城区一模)现有含杂质的氧化铜样品(杂质不参加反应),为了测定该样品中氧化铜的质量分数,某同学称取12.5g样品,并用如图所示的装置进行实验,得到如下两组数据:| 反应前 | 氧化铜完全反应后 | |
| 第一组 | 烧杯和澄清石灰水的总质量180.0g | 烧杯和烧杯内物质的总质量184.3g |
| 第二组 | 玻璃管和氧化铜样品的总质量是44.5g | 玻璃管和管内物质的总质量是42.9g |
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com