天然水中一般都溶有Ca(HCO
3)
2、Mg(HCO
3)
2等物质,在加热条件下,这些溶解的物质会变成溶解度更小的碱和碳酸盐等其它物质,所以热水壶中常会形成由碱和碳酸盐等组成的水垢.某研究性学习小组的同学对水垢的成分进行了如下研究.
【研究课题】探究热水壶底部水垢的主要成分
【查阅资料】该小组同学通过查阅资料知道,天然水中一般都含有Ca
2+、Mg
2+、HCO
3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐、碱等的混合物).同时,他们还查阅到下列有关物质的溶解性:
| 物 质 |
Ca(HCO3)2 |
Mg(HCO3)2 |
Ca(OH)2 |
Mg(OH)2 |
CaCO3 |
MgCO3 |
| 溶解性 |
可溶 |
可溶 |
微溶 |
不溶 |
不溶 |
微溶 |
【提出猜想】水垢的主要成分一定含有Mg(OH)
2和CaCO
3,可能含有Ca(OH)
2和
.
【设计方案】(1)甲同学对是否含有Ca(OH)
2进行了实验,请你帮他完成实验报告:
| 实验操作 |
实例现象 |
实验结论 |
|
|
水垢中无Ca(OH)2 |
(2)乙同学设计如图1所示的装置,利用一定量的水垢与足量的稀盐酸反应,待产生气泡停止后,测量B装置增加的质量,从而推出混合物的组成.这种方案受到丙同学的反对,其反对的理由是
.
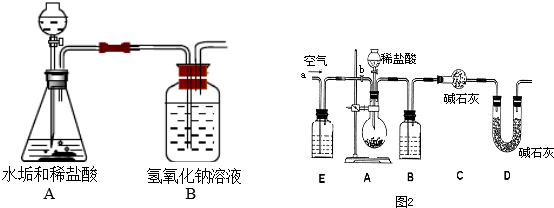
(3)丁同学将装置进行了改进,采用图2所示装置进行实验.其主要实验步骤如下:
①按图组装仪器,将25g水垢试样放入烧瓶中,加入足量盐酸溶液;
②测量一定时间内C装置增加的质量;
③待锥形瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气;
④再次称量C装置增加的质量;
⑤重复③和④的操作,直至C装置中物质质量不变;
⑥测得C装置增加的质量为12g.
①B、E装置中所盛试剂分别为
.
②待烧瓶中不再产生气泡时,打开活塞b,从导管a处缓缓鼓入一定量的空气,其目的是
.
【实验结论】根据上述信息你认为该水垢的成分是
(写化学式)

