
题目列表(包括答案和解析)
| 20mL×1.18g/cm3×37% |
| 20mL×1.18g/cm3+60mL×1.0g/cm3 |
| 20mL×1.18g/cm3×37% |
| 20mL×1.18g/cm3+60mL×1.0g/cm3 |
| 实验步骤 | 实验现象和结论 |
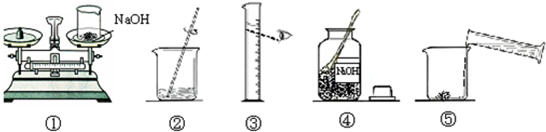
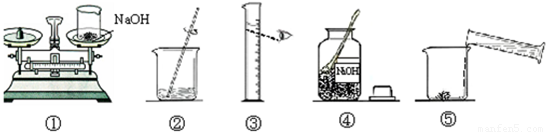
分别取等量三种溶液于三支试管中,滴加酚酞试液; 2、向未变红的两支试管中继续滴加鉴别出的氢氧化钠溶液. 分别取等量三种溶液于三支试管中,滴加酚酞试液; 2、向未变红的两支试管中继续滴加鉴别出的氢氧化钠溶液. |
一支试管中溶液变为红色,另外两支不变色.变红的为氢氧化钠溶液; 滴入相同滴数的氢氧化钠,一支试管中的溶液先变成红色,溶液先变红的是溶质质量分数为5%的盐酸,然后继续滴向另外一支继续滴加氢氧化钠溶液后变红.后变红的是溶质质量分数为10%的盐酸. 一支试管中溶液变为红色,另外两支不变色.变红的为氢氧化钠溶液; 滴入相同滴数的氢氧化钠,一支试管中的溶液先变成红色,溶液先变红的是溶质质量分数为5%的盐酸,然后继续滴向另外一支继续滴加氢氧化钠溶液后变红.后变红的是溶质质量分数为10%的盐酸. |
实验室用溶质质量分数为10%氢氧化钠溶液进行水的电解实验.
实验一:配制100g溶质质量分数为10%氢氧化钠溶液.
(1)所需的氢氧化钠质量: g;
(2)称量时,氢氧化钠固体应放于天平 (填“左”或“右”)盘的烧杯内;量取的需的水(水的密度为1g/cm3),应选择的量筒的规格是 mL(选填“10”、“100”或“250”).
实验二:水的电解实验
用如图装置进行水的电解实验.已知氢氧化钠在水的电解实验中,只起到增强水的导电性作用.
(3)开始反应前a,b两管内都充满溶液.关闭活塞,接通电源,一段时间后,两管产生的气体如图所示,则a管下方导线应接电源的 极(填“正”或“负”).用 验证b管中的气体,写出电解水的化学方程式: .
(4)说明水是一种化合物的实验事实: .
(5)电解后溶液的溶质质量分数 10%(填“<”、“=”或“>”).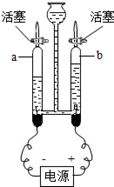
实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数。
(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为 g,水的体积为 mL(水的密度近似看作1g/cm3)。
 (2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)
测定溶液的pH,得到的数据如下:
| 加入氢氧化钠 的体积/mL | 0 | 1.0 | 8.0 | 9.5 | 10.5 | 12.0 | 16.5 |
| 烧杯中溶液pH | 1.0 | 1.3 | 2.0 | 3.9 | 9.9 | 11.9 | 12.8 |
依据表中数据绘制出烧杯中溶液的pH与加入氢氧
化钠溶液体积(V)之间的变化关系图。
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为 mL,A点所表示的溶液中溶质的化学式为 。
(4)计算此瓶盐酸的溶质质量分数。(请写出计算过程。氢氧化钠溶液的密度按1.0g/mL计算)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com