化学小组同学在课外读物中看到:“通常CO
2可作灭火剂,但有些物质(如Na)着火,不能用CO
2熄灭.”他们决定探究CO
2与Na反应的产物.
【提出猜想】CO
2与Na反应可能生成4种物质:C、CO、Na
2O、Na
2CO
3.
【查阅资料】①Na是非常活泼的金属,常温下与O
2、H
2O等物质反应.②碱性的Na
2CO
3溶液与中性的CaCl
2溶液发生复分解反应.③Na
2O是白色固体,与H
2O反应生成NaOH.
④向氯化钯(PdCl
2)溶液中通入CO,产生黑色沉淀.
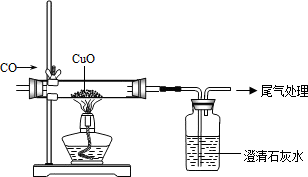
【实验过程】同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)
(1)实验记录
| 序号 |
实验操作 |
主要实验现象 |
实验结论和解释 |
| ① |
打开a,关闭b,由长颈漏斗注入稀盐酸 |
A中产生大量气泡
E中出现浑浊 |
A、E中反应的化学方程式分别为
CaCO3+2HCl=CaCl2+H2O+CO2↑ CaCO3+2HCl=CaCl2+H2O+CO2↑ 、
CO2+Ca(OH)2=CaCO3↓+H2O CO2+Ca(OH)2=CaCO3↓+H2O |
| ② |
当E中出现混浊时,打开b,关闭a,点燃酒精灯 |
D中Na剧烈燃烧,产生白烟内壁附着黑色、白色固体;G中产生黑色沉淀 |
反应产物一定有
C和CO C和CO |
| ③ |
取D中白色固体于试管中,加水溶解,再加入石灰水 |
产生白色沉淀 |
反应产物还有
Na2CO3 Na2CO3 |
(2)实验反思①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是
排出装置中的空气,防止空气的干扰
排出装置中的空气,防止空气的干扰
.
②装置C中为浓硫酸,若无装置C,对实验有影响的物质是
水
水
.
③装置G中气球的作用是
回收尾气
回收尾气
.
④装置B是除杂装置,其中的溶液选用NaHCO
3溶液而不用NaOH溶液的原因是:
盛有饱和NaHCO3溶液的洗气装置可以吸收HCl,不与CO2反应;但氢氧化钠溶液虽吸收HCl,也会与二氧化碳反应
盛有饱和NaHCO3溶液的洗气装置可以吸收HCl,不与CO2反应;但氢氧化钠溶液虽吸收HCl,也会与二氧化碳反应
.
⑤检验第4种物质是否存在的实验方案:取D中白色固体于试管中,
加水完全溶解,加入过量CaCl2溶液至不再产生沉淀,滴加酚酞试液,溶液呈红色.说明白色固体中含Na2O
加水完全溶解,加入过量CaCl2溶液至不再产生沉淀,滴加酚酞试液,溶液呈红色.说明白色固体中含Na2O
.