
题目列表(包括答案和解析)
3.除去Cl2中混有的少量HCl气体,可将气体通入 ( )
A.苛性钠溶液 B.饱和NaHCO3溶液
C.澄清石灰水 D.饱和氯化钠溶液
2.将氯气制成漂白粉的主要目的是:①使它转变为较易溶于水的物质 ②转变为较稳定,
便于贮存的物质 ③提高氯的百分含量 ④提高漂白能力
A.①② B.②③ C.①②④ D.只有②
1.下列关于氯气的说法中正确的是 ( )
A.双原子分子,易溶于水 B.黄绿色不易液化的气体
C.单质的密度大于空气 D.与铁反应的产物是FeCl2
30.(7分)用200mL密度为1.84g/cm3 、H2SO4的质量分数为98%的浓硫酸与等体积的水混合,配得一定体积的稀硫酸。
(1)所得稀硫酸中H2SO4的质量分数是 49% (填“﹥”、“﹤”或“=”)。
(2)浓硫酸中H2SO4的物质的量浓度是多少?
级上期期未考试
29.(6分)将8.7gMnO2与足量的浓盐酸混合,在加热条件下,使其完全反应。计算:
(1) 所得Cl2在标准状况下的体积;
(2) 被还原的HCl的物质的量。
28.(7分)已知A、B、C、D四种物质的转化关系如下:
①
3A+6KOH(浓溶液) 5B+C+H2O
5B+C+H2O
②
②C 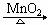 B+D↑
B+D↑
③ C + HCl (浓)→A↑ +B + H2O ,且A,D均为单质。(②③反应均末配平)
(1)由此推断A、C的化学式为:A ,C 。
(2)写出反应①的化学方程式,并标出电子转移的方向和数目:
27.(12分)W、X、Y、Z四种化合物的焰色反应均为黄色,它们之间有下列变化关系:
①W 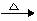 X+CO2↑+H2O ②Z+CO2→X+O2
X+CO2↑+H2O ②Z+CO2→X+O2
③Z+H2O→Y+O2 ④X+Ca(OH)2(饱和石灰水)→Y+CaCO3↓
据此:W、Z的化学式分别是 、 ,反应②的化学方程式是
,反应④的离子方程式是 。
26.(6分)在淀粉碘化钾溶液中滴入少量次氯酸钠溶液,并加入少量稀硫酸,溶液立即变蓝,其反应的离子方程式为 ;在上述蓝色溶液中加入足量的亚硫酸钠溶液后,蓝色逐渐消失并有硫酸根离子生成。由以上实验事实可得ClO-、I2、SO42-的氧化性由强到弱的顺序是
。
24.(6)分某同学拟用H2SO4的质量分数为98%的浓硫酸(p=1.84g/cm3)配制1mol/L的稀硫酸100mL,请回答下列问题:
(1)应量取浓硫酸的体积为 mL。
(2)可供选择的仪器有:①玻璃棒;②胶头滴管;③100mL容量瓶;④托盘天平;⑤50mL烧杯;⑥10mL量筒;⑦100mL量筒;请选出要使用的仪器的序号: 。
(3)如果该同学在定容时俯视刻度线,其它操作均正确,则所配制溶液中H2SO4的物质的量浓度
1mol/L(填“>”、“<”或“=”)。
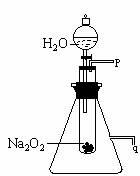 25.(10分)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉燃烧起来。
25.(10分)用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,可观察到脱脂棉燃烧起来。
(1) 由实验现象所得出的有关Na2O2和H2O反应的结论是:
a.该反应放出气体的名称是 。
b.该反应是 热反应(填“吸”或“放”)。
(2) 某研究性学习小组拟用右图的装置进行实验以证明上述结论。
① 用以验证结论a的实验方法及现象是:
。
② 用以验证结论b的实验方法及现象是:
.。
23. 在200℃时,11.6gCO2和H2O(气)的混合气体与足量的Na2O2充分反应后,固体质量增加了3.6g,则原混合气体的平均相对分子质量为
A. 5.6 B. 16.2 C . 23.2 D. 46.4
高一级上期期末考试
化学试卷
第I卷答题栏
第II卷(非选择题 共54分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com