
题目列表(包括答案和解析)
1、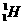 、
、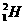 、
、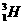 、H+、H2是
、H+、H2是
A、氢的五种同位素 B、五种氢元素 C、氢的五种同素异形体 D、氢元素的五种不同粒子
33、含有碳酸钠、碳酸氢钠、过氧化钠的固体混合物35.2克,加热使其充分反应后,产生的气体全部通入12.4克氧化钠中充分反应,固体质量变为14.2克,在此固体中加入盐酸不产生气体。将35.2克混合物加热后的残留固体冷却称量为31.8克的纯净物,求原混合物中各物质的质量。
32、将一块重2.92克的表面被氧化的金属钠(氧化物按氧化钠计),投到97.08克水中,产生0.1克气体,试求:
(1)未被氧化的金属钠的质量
(2)所得溶液中溶质的质量分数
31、有四种某碱金属元素的化合物W、X、Y、Z,已知它们进行焰色反应时火焰呈紫色(透过蓝色钴玻璃观察)。根据以下反应式推测并写出各物质化学式及指定反应的离子方程式:(己知Y中两元素原子个数比1:1)(1)W=X+CO2↑+H2O (2)Y+CO2=X+O2
(3)Y+H2,O=Z+O2↑ (4)X+Ca(OH)2=Z+CaCO3↓
写出下列物质化学式:W X Y Z
写出离子方程式:
Y+H2O
Z+CO2
30、要鉴别KNO3和NaNO3固体,应利用 方法。
29、将NaHCO3固体在试管中加热,将产生的气体依次通过足量的Na2O2固体。浓硫酸,最后得到的气体是 。
28、除去下列物质中所含少量杂质(括号内为杂质)的方法是(用化学方程式表示):(3)(4)小要求写出离子方程式
(1)Na2O2((Na2O)
(2)Na2CO3固体(NaHCO3固体)
(3)KCl溶液(K2CO3)
(4)NaHCO3溶液(Na2CO3)
27、在K2Cr2O7+14HCl=2KCl+2CrCl3+3Cl2↑+7H2O反应中,是氧化剂,是还原剂,元素被氧化,元素被还原,HCl现的性质是-。在方程式上标注电子转移数目和方向。
26、Na2O是 色固体,与水反应的化学方程式为,
制备Na2O通常采用的方法是:2NaNO2+6Na=4Na2O+N2↑。不采用钠在氧气中燃烧的方法而采用此方法是因为。
25、碱金属元素包括(填符号) 等六种元素。随核电荷数增多,它们的沸点逐渐 。它们的原子最外层都有 个
电子,易 电子,所以它们表现出很强的 性。随着核电荷数增多,它们的原子半径逐渐 ,失电电能力逐渐 ,所以元素金属性逐渐 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com