
题目列表(包括答案和解析)
5.通常情况下,氧气是一种_________、___________的气体。可燃物在氧气中燃烧通常比在空气中_____________。许多物质都会与氧气发生反应,动植物的新陈代谢、__________、_________________等过程都含缓慢氧化。氧气的重要用途是_________和_________。
4.随着工业生产和交通运输业的迅速发展,排放到空气中的_______和_______大大增加,造成了空气污染。目前,我国重点城市空气质量日报的监测项目中不包括( )。
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.总悬浮颗粒物
3.只由一种物质组成的物质叫_______,如___________。由两种或两种以上物质混合而成的物质叫___________,如____________。
2.经测定,空气中各组分气体的体积分数大致为是________占78%,_____占21%,稀有气体占_______,二氧化碳占_________,其他气体和杂质占______。
1.自然界氧气产生的途径是____________________,消耗氧气的途径有_________、_______________,因此自然界里氧气的含量基本保持不变。
26.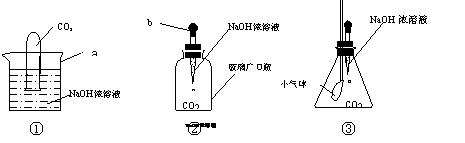 小明在探究CO2和NaOH是否发生反应时,设计出下列三种装置进行实验:
小明在探究CO2和NaOH是否发生反应时,设计出下列三种装置进行实验:
请回答以下几个问题:
(1)写出上图中标有字母的仪器名称:a ,b 。
(2)以上三个实验中,①③有明显现象,请你帮小明记录他观察到的实验现象:
实验① 。实验③ 。
(3)实验②因选用仪器不当导致未能观察到明显现象,请你帮小明寻找一种物品替代该装置中的广口瓶,以使实验取得成功,你将选用的物品是 ,改进后能看到的实验现象是 。
(4)请你进一步设计实验来检验CO2和NaOH溶液反应生成了Na2CO3,并将有关的实验操作、现象、结论填入下表:
|
实验操作 |
实验现象 |
结 论 |
|
|
|
|
25.某学习小组用图示装置测定黄铜屑(锌铜合金)的组成,取一定量的黄铜屑放入烧杯中,并加入足量稀硫酸。不同时间电子天平的读数如下表所示(不考虑H2O逸出):
|
反应时间/min |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
烧杯及所盛物 质总质量/g |
335.70 |
335.54 |
335.44 |
335.38 |
335.34 |
335.32 |
335.31 |
335.30 |
335.30 |
(1) 反应生成H2的总质量为_______________g。
(2) 若要计算黄铜屑中锌质量分数,还缺少的数据是____________,若该数据用a表示,求出黄铜屑中锌的质量分数(写出计算过程)
24.在高温下赤热的焦炭能与水蒸气发生反应,对其反应后的生成物,甲、乙、丙三位同学作了如下猜想:甲认为有H2、CO生成;乙认为有H2、CO、CO2生成;丙认为除有H2、CO、CO2生成外,可能还有其它的含碳化合物生成。
(1)探究小组组长丁认为三位同学的猜想均存在其合理性,请你从原子-分子论的观点解释他们猜想的合理性。________________________________。
(2)乙同学为了证明他的猜想是正确的,设计了如下实验,实验装置图如下:
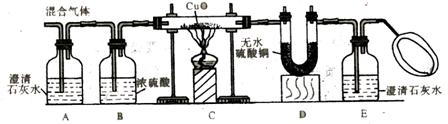
①___________________________现象证明含有CO2;
②___________________________现象证明含有H2;
③___________________________现象证明含有CO。
(3)E装置后的气球有什么用?_________________________________________________
23.甲同学在某食品包装袋内,发现有一个装有白色颗粒状固体A的小纸袋,上面写着“生石灰干燥剂,请勿食用”。甲同学随手将小纸袋拿出来放在空气中,经过一段时间后,发现纸袋内的白色颗粒粘在一起成为块状固体B。请与甲同学一起对块状固体B进行探究。
(1)猜想一:块状固体B中除氧化钙外还可能有__________、__________。
写出白色颗粒状固体A在空气中转变成块状固体B的有关化学反应方程式:_________
________________________。
(2)猜想二:块状固体B溶于水可能有__________现象(填“放热”或“吸热”)。请设计实验方案验证你的这一猜想(至少写出两种方案,如果写出三种正确方案奖励1分)
①________________________________________________________;
②_______________________________________________________;
③______________________________________________________。
(3)取适量块状固体B加入盛有一定量水的试管中,振荡、静置、过滤,得到少量白色固体C。就白色固体C的成分,甲同学与乙同学进行讨论,一起猜想。甲同学认为,白色固体C可能是氢氧化钙;乙同学认为,白色固体C可能是碳酸钙;你认为,白色固体C,还可能是_________________________。
请设计一个实验验证你的猜想(填写下表):
|
方
案 |
现象和结论 |
|
|
|
22.小明同学在学习酸的性质时,他用大小、外形均相同的铝片分别和H+浓度相同的稀盐酸、稀硫酸反应。他意外地发现:铝片与稀盐酸反应放出气泡的速度明显快于与稀硫酸反应放出气泡的速度。是什么原因导致了反应现象的差异呢?小明从微观角度分析得出,H+浓度相同的盐酸、硫酸中,只是所含_____________不同。
小时提出了如下猜想:
①Cl-能促进铝和酸的反应,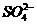 对反应无影响;
对反应无影响;
②Cl-对反应无影响,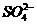 能抑制铝和酸的反应;
能抑制铝和酸的反应;
③Cl-能促进铝和酸的反应,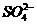 能抑制铝和酸的反应。
能抑制铝和酸的反应。
他进行了如下实验探究:
|
组别 |
相同的铝片 |
H+浓度 相同的酸 |
反应片刻后添加 某种试剂(少量) |
添加试剂后的反应现象 |
结 论 |
|
1 |
1g铝片 |
5mL |
Na2SO4 |
无明显变化 |
_____和_____离子对反应无影响 |
|
2 |
1g铝片 |
5mL |
NaCl |
明显加快 |
_____离子对反应有促进作用 |
针对上述探究过程回答下列问题:
(1)请你将表格中的空格补充完整。
(2)上述猜想____________是成立的。
(3)若将第2组实验中添加的试剂NaCl改为HCl气体,能否完成探究任务?请说明原因。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com