
题目列表(包括答案和解析)
29、(8分)有三种白色粉末,分别是碳酸钠、氯化铁和氯化钠中的一种。请设计一个实验方案,把这三种粉末区分开来。叙述实验操作、预期现象和结论。
|
实验操作 |
预期现象与结论 |
|
|
|
|
|
|
28、(14分)小强和小明两位同学在实验室用下列装置制取几种气体。
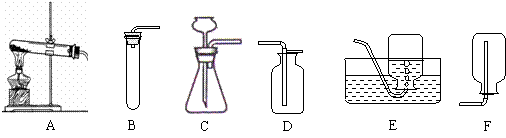
⑴ 小强想用高锰酸钾制取一瓶尽可能纯净的氧气,他应选择上述装置中的A和
(填装置序号)进行组装,而小明认为A装置中还缺少 ;
⑵ 在装入药品前,应先检查装置 ;
⑶(2分)小强用15.8g高锰酸钾(化学式KMnO4)制取氧气,完全反应后理论上可以生
成氧气的质量为 g;
⑷ 当氧气收集满并取出集气瓶后,停止制取氧气实验的正确操作步骤是先
,后 。
⑸ 小明要制取少量CO2,他选用的气体发生装置是(填装置序号) ,收集CO2的装置是(填装置序号) ,选用该收集装置的理由是
,检验集气瓶中是否收集满CO2的方法是
。
⑹ C装置中长颈漏斗的作用是便于 。为了防止生成的气体从长颈漏斗逸出,必须使长颈漏斗 。
27、(6分)某同学设计了一套验证碳酸具有酸性而二氧化碳没有酸性的实验。他首先用紫色石蕊试液浸泡滤纸,晒干后折成纸花,然后按下图所示分别进行:
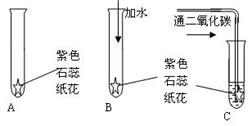
⑴往紫色石蕊纸花喷上稀醋酸,紫色石蕊纸花显________色;
⑵在B实验中,当加入水后,紫色石蕊纸花显________色,B实验的作用是______________;
⑶在C实验中,紫色石蕊纸花变_____色,这一实验结果说明____________;
⑷通过以上实验,尚未达到验证的目的,若要达到验证的目的,你的方法是_________。
26、(2分)
(1)用PH试纸测定液体的PH值时,所需用品除了玻璃棒,PH试纸外,还需要 ;
(2)用量筒量取一定体积液体时,需要注意的事项是 。
25、(9分)碳酸钠用途非常广泛,是工业生产中重要的化工原料。在1921年我国科学家 侯德榜创造了一种著名的纯碱生产方法--“联合制碱法”。
“联合制碱法”生产过程:
(1)第一步主要反应为NH3+CO2+H2O = NH4HCO3 该反应属于 反应基本反应类型。
(2)第二步用食盐与NH4HCO3反应。食盐来源于某盐田,该粗盐主要含有氯化钠,此外还含有少量硫酸钠,氯化钙和氯化镁。经净化、精制得到生产碳酸钠所需要的食盐水,其主要流程如下:
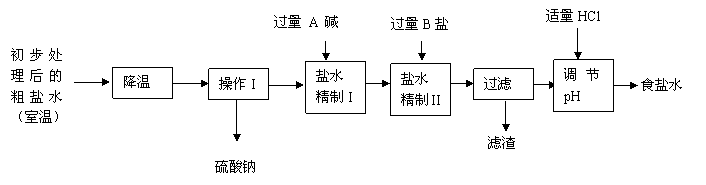

①通过降温使硫酸钠从粗盐水中析出,其原理是氯化钠
和硫酸钠的溶解度与温度的变化差异较大,请在溶解度图
(如右图)中简单画出氯化钠和硫酸钠的溶解度曲线变化趋势图。
②“精制I”操作中,加入过量含钙元素的碱的化学式是 。
其反应化学方程示为 。
③“精制II”操作中,加入B盐的有关反应方程式为 。
④为保证“精制II”操作中过量B盐把杂质全部除去,请在下表中写出检验溶液中B盐是否过量的实验报告。
|
实验操作 |
实验现象 |
实验结论 |
|
|
|
|
⑤查阅资料得知NaCl 、NH4HCO3、 NaHCO3 、NH4Cl在30℃时的溶解度如下表所示:
|
温度 |
NH4Cl |
NH4HCO3 |
NaHCO3 |
NaCl |
|
30℃ |
41.1g |
27.0g |
11.1g |
36.3g |
请根据溶解度表所提供的信息,写出“联合制碱法”中的第二步属于复分解反应的化学方程式: 。
(3)第三步处理制得碳酸钠,反应原理为2NaHCO3 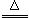 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
24、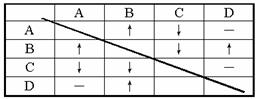 (6分)现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠4瓶失去标签的溶液, 分别编号为A、B、C、D。每次取少量溶液两两混合,所观察到的现象记录在下表中(“-”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)。由此推断4瓶溶液中的溶质的化学式分别为:
(6分)现有稀盐酸、稀硫酸、氢氧化钡、碳酸钠4瓶失去标签的溶液, 分别编号为A、B、C、D。每次取少量溶液两两混合,所观察到的现象记录在下表中(“-”表示无明显现象;“↓”表示有沉淀生成;“↑”表示有气体生成)。由此推断4瓶溶液中的溶质的化学式分别为:
A. ;B. ;C. ;D.
写出上述实验过程的有关反应方程式:
A+B
C+D
23、 (6分)将下列两组中的两种反应物混合,回答下列问题:
(1)根据实验事实完成下表(没有发生反应的,化学方程式一栏“/”)
|
编号 |
反应物1 |
反应物2 |
现象 |
化学方程式 |
|
1 |
稀盐酸 |
氢氧化铜 |
|
|
|
2 |
稀硫酸 |
氢氧化钡溶液 |
有白色沉淀生成 |
|
|
3 |
稀硝酸 |
澄清石灰水 |
没有明显现象 |
|
(2)分析上述实验,反应能够发生的共同原因是:反应物1中都含有(填化学用语,下同)___________,反应物2中都含有___________。
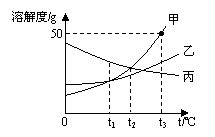
22、(5分)右下图是甲、乙、丙三种固体物质的溶解度曲线,请根据图示填空:
(1)在______℃时,甲与丙的溶解度相等。
 (2)t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶
(2)t3℃时,甲物质的饱和溶液中,溶质、溶剂、溶
液的质量之比为___ _______。
(3)t1℃时,甲、乙、丙三种物质的饱和溶液中,溶
质质量分数的大小关系是________________(用“甲”、
“乙”、“丙”及“>”、“<”或“=”表示)。
(4)从右图你能获得的信息有(写两条)
21、(4分)用化学用语填空:
(1)一个甲烷分子 ; (2)2个氢离子 ;
(3)氧化铁 ; (4)硫酸铵 ;
20、A、B、C、D是四种金属单质,A能从B的硝酸盐溶液中置换出B,但A不能与稀盐酸反应。相同条件下,C、D能与稀盐酸反应产生H2,且D比C反应剧烈。则四种金属的活动性由强到弱的顺序是( )
A.A、B、C、D B.B、A、C、D
C.D、C、A、B D.D、C、B、A
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com