
题目列表(包括答案和解析)
3、在一定环境中,常温常压下的水可以瞬间结成冰,俗称”热冰”。下列说法正确的
A.”热冰”是纯净物 B.“热冰”在任何条件下都不会熔化
C.“热冰”与水的化学性质不同 D.结成“热冰”后,分子停止运动
2、搜救人员克服严重的高原反应等困难,全力展开搜救。吸氧是克服高原反应的方法之一,吸氧可以帮助搜救人员的高原反应的原因是
A. 氧气可供呼吸 B. 氧气可以燃烧
C.氧气可以支持燃烧 D.氧气是无色无味的无毒气体
1、下列常见物质的用途,主要利用其物理性质的是

A.压缩天然气做燃料 B.金属铜用于制导线 C.氮气用于食品防腐 D.石灰中和酸性土壤
2、步骤②通入氮气的目的是: ▲
[实验结论]
该绿色粉末的组成元素是: ▲ ;各元素的质量比为: ▲ (写出计算过程)
1、老师看了实验方案后认为,从环保的角度来看,此装置有一个缺陷,建议装置D后还应添加一个酒精灯,并在实验步骤 ▲ (填实验步骤的序号)中点燃
28.聪聪同学在实验室帮老师整理废弃药品时发现一瓶没有标签的绿色粉末,对其组成很好奇。征得老师允许后,设计了以下实验进行探究。
|
操作步骤 |
实验现象 |
结论或化学反应方程式 |
|
取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连。 |
①产生大量气体,使石灰水变浑浊。 ②样品全部溶解,溶液呈蓝色。 |
①样品中含有 ▲ 离子 ②样品中含有 ▲ 离子 |
|
在上述蓝色溶液中,插入一根洁净的铁丝。 |
①铁丝表面缓缓产生少量气泡。 ②片刻后铁丝表面出现红色物质。 |
① ▲
② ▲ (均用方程式表示) |
为了进一步确定该物质的元素组成,查阅部分资料后,他继续进行了实验。
[资料查阅]白色的无水硫酸铜可做吸水剂,遇水会变成蓝色。
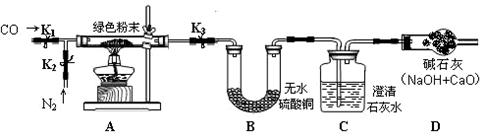 [实验步骤]
[实验步骤]
①如图搭建实验仪器,并检验装置的气密性。
②在A装置中装入11.1g绿色粉末。关闭K1,打开K2、K3,持续通入适量N2。
③关闭K2、K3,分别称量装置B、C、D的质量,记录数据。
④打开K3,点燃酒精灯加热绿色粉末直至装置C中无气泡产生时,关闭K3,熄灭酒精灯。分别称量装置B、C、D的质量,记录数据。
⑤待A冷却后,打开K1、K3,持续通入适量CO,再次点燃酒精灯加热。
⑥当A中粉末全部变红后,熄灭酒精灯。试管冷却后,关闭K1。称量装置A、B、C、D的质量,记录数据。
[实验现象和数据处理]
|
|
装置A |
装置B |
装置C |
装置D |
|
第一次 加热后 |
绿色粉末变黑色 |
▲ 质量增加0.9g |
出现白色沉淀, 质量增加2.2g |
无明显变化 质量不改变 |
|
第二次 加热后 |
黑色粉末变红色 质量为6.4g |
无明显变化, 质量不改变 |
沉淀先增加后部分溶解; 质量增加 |
无明显变化 质量不改变 |
[实验分析与反思]
27.(7分)实验室需配制4%的氢氧化钠溶液200g,并用此溶液测定某敞口放置一段时间的盐酸的溶质质量分数。
(1)配制200g质量分数为4%的氢氧化钠溶液,需要氢氧化钠固体的质量为 ▲ g,水的体积为 ▲ mL(水的密度近似看作1g/cm3)。
 (2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
(2)取10g此盐酸于烧杯中,逐滴滴加溶质质量分数为
4%的氢氧化钠溶液,用pH计(一种测定溶液pH的仪器)
测定溶液的pH,得到的数据如下:
|
加入氢氧化钠 的体积/mL |
0 |
1.0 |
8.0 |
9.5 |
10.5 |
12.0 |
16.5 |
|
烧杯中溶液pH |
1.0 |
1.3 |
2.0 |
3.9 |
9.9 |
11.9 |
12.8 |
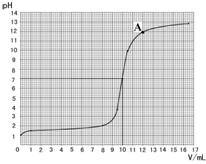
依据表中数据绘制出烧杯中溶液的pH与加入氢氧
化钠溶液体积(V)之间的变化关系图。
(3)根据上图查出氢氧化钠与盐酸恰好完全反应时,所滴加氢氧化钠溶液的体积为 ▲ mL,A点所表示的溶液中溶质的化学式为 ▲ 。
(4)计算此瓶盐酸的溶质质量分数。(请写出计算过程。氢氧化钠溶液的密度按1.0g/mL计算) ▲
26.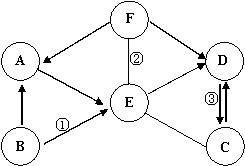 (4分)A-F均为生活中常见的物质。其中A与B的元素组成相同,C与D的元素组成相同;A、B、C、D的类别相同,C、D、E、F
(4分)A-F均为生活中常见的物质。其中A与B的元素组成相同,C与D的元素组成相同;A、B、C、D的类别相同,C、D、E、F
在常温下的状态相同。其物质间的转化关系如
图所示,图中“--”表示两端的物质能发生
 化学反应;“ ”表示物质间存在转化关系,
化学反应;“ ”表示物质间存在转化关系,
其余反应条件、部分反应物和生成物均已略去。
试推断:
(1)D物质的一种主要用途____▲______。
(2) 写出下列化学方程式:
反应①:_____________▲_____________________________;
反应②:____________▲______________________________;
反应③:____________▲_______________________________;
25.(6分) 2011年3月22日是第十九届“世界水日”。今年世界水日的主题是 “城市用水:应对都市化挑战”。
南京目前还是地下管网雨污合流。平时,浪费了污水处理设施的处理能力;每逢暴雨,为了尽快泄洪直接排水,又导致秦淮河、玄武湖的水质骤然变差。为此,南京投资183亿元打造雨污分流工程,雨水补充河道,污水进入污水治理厂处理,治水经济集约。
 (1)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,
其中净化程度最高的方法是 ▲ 。
(1)天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,
其中净化程度最高的方法是 ▲ 。
(2)硬水给生活和生产带来很多麻烦,生活中可用 ▲ 来区分硬水和软水,常用 ▲ 的方法来降低水的硬度。
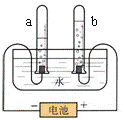
(3)右图是电解水实验装置。a管产生的是___▲__。请写出水在通电条件下反应的化学方程式 ▲ 。
(4)保护水环境、珍爱水资源,是每个公民应尽的责任和义务。下列做法有利于保护水资源的是 ▲ (填序号)。
A.大量使用化肥农药 B.工业废水处理达标后排放
C.推广使用无磷洗衣粉 D.生活污水直接排放
24.(10分)3月11日,日本仙台港以东发生大地震。受其影响,当地时间12日下午,日本福岛第一核电站1号机组内发生氢气爆炸。
(1)机组内氢气的来源是:冷却系统被破坏后,核燃料棒外由锆(Zr)合金做的包壳被加热到1200℃以上时,和水发生反应,生成氧化锆(ZrO2),并放出氢气。氧化锆中锆的化合价为___▲____; 氢气爆炸的化学方程式为______▲____________。
(2)实验室常用锌粒和稀硫酸来制取氢气,反应的化学方程式为_________▲__________;可以选择下图中 ▲ (填装置序号)做发生装置;装置A中的玻璃仪器有导管、_▲____和 _▲__(填仪器名称)
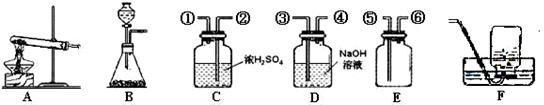
(3)高阳同学用锌粒和浓盐酸制取氢气,制得的氢气含有少量的水蒸气和HCl气体。若要得到干燥、纯净的氢气,需要通过C和D装置,则装置按导管口数字连接的顺序是:发生装置 → ▲ → ▲ → ▲ → ▲ →收集装置。装置E是用排空气法收集氢气的装置,请你判断气体应由 ▲ 进 ▲ 出 (填导管口序号)。
(4)实验室常用加热无水醋酸钠和碱石灰两种固体混合物制取甲烷气体,则制取甲烷可以选用的发生装置是__▲____;如用F装置收集甲烷,实验结束时,停止该实验的正确的操作方法是_____________▲____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com