
题目列表(包括答案和解析)
2.对于可逆反应2SO2+O2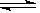 2SO3,在混合气体中充入一定量的18O2,足够长时间后, 18O原子
2SO3,在混合气体中充入一定量的18O2,足够长时间后, 18O原子
A.只存在于O2中 B.存在于SO2、O2和SO3中
C.只存在于O2和SO2中 D.只存在于O2和SO3中
1.下列说法不正确的是
A.催化剂能改变化学反应速率,但不能使化学平衡发生移动
B.参加反应的物质的性质是决定化学反应快慢的主要因素
C.反应物分子(或离子)间的碰撞是发生反应的先决条件
D.增大反应物浓度,可增大活化分子的百分数,所以反应速率加快
22.(4分)盖斯定律在生产和科学研究中有很重要的意义,有些反应的反应热虽然无法直接测得,但可通过间接的方法测定,现根据下列3个热化学反应方程式:
① Fe2O3(s)+3CO(g)== 2Fe(s)+3CO2(g) △H=-24.8 kJ•mol-1
② 3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=-47.2 kJ•mol-1
③ Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H=+640.5 kJ•mol-1
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式 。
21. (11分)某燃料电池以熔融K2CO3(其中不含O2-,HCO3-)为
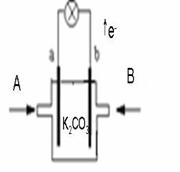
(11分)某燃料电池以熔融K2CO3(其中不含O2-,HCO3-)为
电解质,以乙烷为燃料,以空气为氧化剂,以具有催化作用和导
电能力的稀土金属材料为电极,该电池简化装置如右图所示,回
答下列问题:
(1)该原料电池的正极是 极,B端入口充入的物质是
(2)写出该原料电池的化学方程式(与乙烷燃烧方程式相同)
负极反应式为
(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中加入一种物质,加入的物质是 。
20. (11分)某学生用右图所示装置证明溴和苯的反应是取代反应而
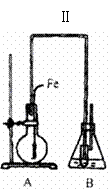
(11分)某学生用右图所示装置证明溴和苯的反应是取代反应而
不是加成反应。主要实验步骤如下:
(1)检查气密性,然后向烧瓶中加入一定量的苯和液溴。
(2)向锥形瓶中加入适量某液体,小试管中加入CCl4,并将右边的
长导管口浸入CCl4液面下。
(3)将A装置中的纯铁丝小心向下插入混合液中。请填写下列空白:
①装置B的锥形瓶中小试管内CCl4的作用是 _;
小试管外的液体是(填名称) ,其作用是 。
②反应后,向锥形瓶中滴加(填化学式)___________溶液,现象
是 ,其作用是 ;装置(Ⅱ)还可起到的作用是 。
19.(8分)利用含淀粉的物质可以生产醋酸。下面是生产醋酸的流程,根据流程回答下列问题:

B是日常生活中有特殊香味的常见有机物,在有些饮料中含有B。
(1)写出化学方程式,并注明反应类型:
I、B与醋酸反应: , 反应。
II、B→C: , 反应。
(2)检验A的试剂和操作: 。
18. (16分)短周期元素T、Q、R、W、Z在元素周期表中的
(16分)短周期元素T、Q、R、W、Z在元素周期表中的
位置如右图所示,其中T所处的周期序数与主族序数相等,
请回答下列问题:
(1)Q的气态氢化物的空间结构为 ,R的气态氢化物与Z的气态氢化物生成盐的电子式为: ,Q、R、W对应氢化物的沸点由高到低排列顺序: ;
(2)Z元素比R元素的非金属性强。能证明这一结论的事实是 (填序号)。
①Z的最高价氧化物的水化物酸性比R的强
②相同条件下,Z单质在水中的溶解性强于R单质
③Z的氢化物水溶液比R的氢化物水溶液酸性强
④Z单质能从R氢化物中置换出R单质
(3)R的氢化物与其气态氧化物(ROx)反应生成对应单质和液态水。已知该反应为放热反应,1mol该氢化物参加反应放热量为QkJ,写出此反应的热化学方程式 。
(4)M是一种常见的金属单质,与元素Z的单质有如下图所示转化关系:
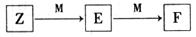
E在溶液中转化为F的离子方程式是 。
若把一定量的M放入E溶液中,完全反应后,所得溶液中E、F的物质的量相等,则已反应的E与未反应的E的物质的量之比为 。
17.(10分)可逆反应a A(g) +b B(g) 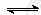 cC(g)
+ dD (g) 。
cC(g)
+ dD (g) 。
(1)将等物质的量A、B、C、D四种物质混合,发生上述反应,当反应进行一段时间后测得A减少了n mol,B减少了n/2 mol,C增加了n/2 mol,D增加了3n/2 mol,此时达到化学反应限度,则化学反应方程式中各物质的系数为;a= ;b= ;c= ;d= ;
(2)取1 mol A和2 mol B置于2 L容器内,在一定条件下发生上述反应,5分钟后测得容器内D的浓度为 0.3 mol ·L-1,这时B的转化率为 ,这段时间内C的反应速率为 ;
(3)若该反应在恒温恒容条件下发生,则可用作判断该反应达到平衡状态的标志是: 。
A.消耗a molA,同时生成d molD B.D的百分含量保持不变
C.容器内气体密度不再发生改变 D.V正(A)=a/c×V逆(C)
16.ag铜、铁的混合物与足量浓硝酸完全反应后,将所得气体与1.68 L O2(标准状况)混合后通入水中,所有气体能完全被水吸收生成硝酸。若向所得溶液中加入足量NaOH溶液至恰好完全沉淀,则最后生成沉淀的质量
A.(a+1.25) B. (a+9.6 )g C.(a+5.1) g D.无法确定
Ⅱ卷 (共60 分)
15.下列离子方程式书写正确的是
A.氯气通入水中:Cl2 + H2O===ClO- + Cl- + 2H+
B.NaHSO4加入NaHCO3溶液中:HSO4-+HCO3-===SO42-+H2O+CO2↑
C.FeBr2中通入足量氯气:2Br-+Cl2===Br2+2Cl-
D.NH4HCO3溶液中加入足量NaOH:NH4++HCO3-+2OH-===NH3·H2O+H2O+CO32-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com