
题目列表(包括答案和解析)
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
实验与探究是化学学习的重要方法和内容。
(1)今年5月,我市各学校进行了实验操作考查。小张同学进行的实验考查是“用稀盐酸鉴别氢氧化钠(NaOH)溶液和碳酸钠(Na2CO3)溶液,并测定碳酸钠溶液的pH”。
①小张同学的实验记录如下表,请补充完整:
| 操作步骤 | 现象记录 | 反应的化学方程式 |
| 取两支试管,分别往试管中加入2mL样品1、2,再往其中滴入盐酸 | 样品1:无明显现象 | ______________________ |
| 样品2:溶液中出现气泡 | ______________________ |

实验室里临时要用NaOH溶液和CO2来制取纯Na2CO3溶液.已知CO2气体通入NaOH溶液过程中极易生成过量NaHCO3,且无明显现象.实验室有下列试剂:
①未知浓度的NaOH溶液 ②37%的盐酸 ③37%的硫酸 ④14%盐酸 ⑤大理石⑥K2CO3固体 ⑦Cu2(OH)2CO3
实验室有下列仪器:铁架台、启普发生器、量筒、烧杯、橡皮管、玻璃导管、分液漏斗.
已知下表中各物质在常温时的溶解度(g/100g水)
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
(1)本实验应选用的仪器除启普发生器、橡皮管、玻璃导管外,还需要______.
(2)为保证制得的Na2CO3溶液尽量纯,应选用的药品(填编号)除①外,还需要______.
(3)简要叙述实验步骤,直到制得纯Na2CO3溶液(仪器安装可省略)____________.
(4)根据给出的溶解度表,求出当NaOH溶液中溶质的质量分数大于多少时,在配制过程中会有晶体析出(写出计算步骤和必要的文字说明)
| Na2CO3 | NaHCO3 | NaCl | Na2SO4 | NaHSO4 | NaOH |
| 15.9 | 8.4 | 35 | 35.5 | 20 | 40 |
实验与探究是化学学习的重要方法和内容。
(1)今年5月,我市各学校进行了实验操作考查。小张同学进行的实验考查是“用稀盐酸鉴别氢氧化钠(NaOH)溶液和碳酸钠(Na2CO3)溶液,并测定碳酸钠溶液的pH”。
①小张同学的实验记录如下表,请补充完整:
|
②用pH试纸测定碳酸钠溶液的酸碱度,简述操作的主要步骤:
。
在实验台上有三瓶未贴标签的溶液,已知分别是碳酸钠溶液、氢氧化钠溶液和稀盐酸。为区别这三种溶液,在老师指导下,兴趣小组的同学把这三种溶液按A、B、C进行编号,然后分别各取适量作为样品加入到三支试管中,进行了如下图所示的探究活动:
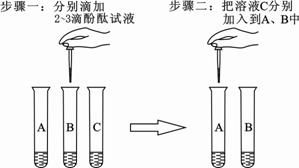
步骤一中,C无明显现象,A、B溶液的颜色变成红色;
步骤二中,A、B溶液的颜色由红色变成无色,且B溶液中有气泡冒出。
①根据上述实验现象可知,B、C溶液分别是_________、__________。
②某小组同学在进行步骤一实验时出现异常现象:往A溶液中加入酚酞试液时,溶液颜色先变成红色,振荡后迅速变成无色。老师指出这是因为溶液浓度过大造成的。接着,老师往该试管的溶液中加入适量盐酸,观察到A溶液的颜色又变成红色,此时溶液中含有的溶质主要是_________________________(酚酞除外)。
一、选择题
1B
二、填空
26.(1) 3 2 (2) 单质 (每空1分,共3分)
27.(1)(C6H10O6)n+nH2O
.files/image018.gif) nC6H12O6
nC6H12O6
(2) C6H12O6
.files/image020.gif)
(3)C2H5OH+3O2
.files/image022.gif) 2CO2+3H2O (每空2分,共6分)
2CO2+3H2O (每空2分,共6分)
28. (1)太阳能(2)水能(3)风能 地热;潮汐能;培养一种特殊的细菌催化分解水等
(任选三种)(每空1分,共3分)
29. CaCO3十2CH3COOH=(CH3COO)2Ca十CO2↑十H2O
30.无 碱性(如NaOH溶液、石灰水、Na2CO3溶液等)在两支盛有A溶液的试管里,分别加入金属铝和铜,观察发生的现象 (每空1分,共3分)
31.(1)FeS+2HCl=FeCl2+H2S ↑ (2分) (2) B、C (1分)
(3)将尾气通入NaOH溶液中或用气球收集后再处理。
(用燃烧的方法处理不给分)((2分)
(4)A、D(1分)
三、实验题〔本题包括2小题,共21分)
32.(l)CaC03+2HCl=CaCl2+CO2↑+H2O
(2)CO2与挤入的NaOH溶液反应,使圆底烧瓶内气体压强减小产生负压,使烧杯里的
NaOH溶液通过导管被压于回底烧瓶内。与剩下的二氧化碳继续反应,进一步产生负压形
成喷泉。
(3)将导管下端插入水中,用手捂住烧瓶,看是否有气泡冒出或在水面下的导管内是
否形成一段稳定的空气柱。
(4)打开止水夹,用手(或热毛巾等)将烧瓶捂热,CO2受热膨胀,赶出玻璃导管内
的空气,再将热源移开,NaOH溶液进入烧瓶内与CO2反应产生负压,即发生喷泉。〔或打开止水夹,将烧瓶冷却,气体体积收缩,产生负压使NaOH溶液进入烧瓶内与CO2反应
即发生喷泉](以上每空2分,共8分)
(5)滴管的橡胶乳头会被NaOH溶液腐蚀,(1分)
33.(1) a:加热时E中有气泡冒出,停止加热后玻璃管内形成一段液柱;(2分)
b:B、E中有气泡冒出,2H2O.files/image024.gif) =2H2O+O2↑ (2分)
=2H2O+O2↑ (2分)
C:C中的红褐色粉末变成黑色;
2Cu+O2.files/image026.gif) =2CuO C+O2
=2CuO C+O2.files/image026.gif) CO2 ↑ (2分)
CO2 ↑ (2分)
(2).files/image029.gif) (2分)
(2分)
(3)水蒸气通过C被D中碱石灰吸收(2分)
洗气瓶 浓硫酸 (或干燥管 碱石灰) (2分)
四、计算
34.解:①设草木灰中K2CO3的质量为x
K2CO3+2HCl=2KCl+H2O+CO2↑
138 144 44
x .files/image031.gif)
.files/image033.gif)
依题意得7.5g-x+.files/image033.gif) =7.5g+45g-45.5g
=7.5g+45g-45.5g
x=0.73g
所以草木灰中K2CO3的质量分数:.files/image036.gif) =9.7%(2分)
=9.7%(2分)
②生成KCl的质量为:.files/image038.gif) =0.79g
=0.79g
反应后所得溶液的溶质质量分数为:.files/image040.gif) =1.7%
=1.7%
答:略。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com