
题目列表(包括答案和解析)
工业上合成氨的反应是:N2(g)+3H2(g)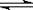 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。
(1)下列事实中,不能说明上述可逆反应已达到平衡的是________
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成n mol N—H的同时生成n mol N≡N
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1︰3︰2
④N2、H2、NH3的体积分数不再改变
⑤混合气体的平均摩尔质量不再改变
⑥混合气体的总物质的量不再改变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
|
时间(h) 物质的量(mol) |
0 |
1 |
2 |
3 |
4 |
|
N2 |
1.50 |
n1 |
1.20 |
n3 |
1.00 |
|
H2 |
4.50 |
4.20 |
3.60 |
n4 |
3.00 |
|
NH3 |
0 |
0.20 |
N2 |
1.00 |
1.00 |
根据表中数据计算:
①反应进行到2小时时放出的热量为________
②0~1小时内N2的平均反应速率________ mol·L-1·h-1;
③此条件下该反应的化学平衡常数K= ________ (保留两位小数)
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向________ 方向移动(填“正反应”或“逆反应”、“不移动”)。
工业上合成氨的反应:N2(g)+3H2(g)  2NH3(g)ΔH=-92.60 kJ·mol-1。
2NH3(g)ΔH=-92.60 kJ·mol-1。
(1)在绝热、容积固定的密闭容器中发生反应:N2(g)+3H2(g)  2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。
2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N—H键的同时生成2n mol H—H键
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
④混合气体的平均摩尔质量增大
⑤容器内的气体密度不变
(2)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | | 1.00 | 1.00 |
工业上合成氨的反应:N2(g)+3H2(g)  2NH3(g)ΔH=-92.60 kJ·mol-1。
2NH3(g)ΔH=-92.60 kJ·mol-1。
(1)在绝热、容积固定的密闭容器中发生反应:N2(g)+3H2(g)  2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。
2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N—H键的同时生成2n mol H—H键
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1∶3∶2
④混合气体的平均摩尔质量增大
⑤容器内的气体密度不变
(2)已知合成氨反应在某温度下2 L的密闭容器中进行,测得如下数据:
时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
NH3 | 0 | 0.20 |
| 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2 h时放出的热量为________ kJ。
②0~1 h内N2的平均反应速率为________ mol·L-1·h-1。
③此温度下该反应的化学平衡常数K=________(保留两位小数)。
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00 mol,化学平衡将向________方向移动(填“正反应”或“逆反应”)。
 2NH3(g)ΔH=-92.60 kJ·mol-1。
2NH3(g)ΔH=-92.60 kJ·mol-1。 2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。
2NH3(g),下列说法能说明上述反应向正反应方向进行的是________(填序号)。| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | | 1.00 | 1.00 |
工业上合成氨的反应是:N2(g)+3H2(g)2NH3(g) ΔH=-92.20 kJ·mol-1。
(1)下列事实中,不能说明上述可逆反应已达到平衡的是________
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成n mol N—H的同时生成n mol N≡N
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1︰3︰2
④N2、H2、NH3的体积分数不再改变
⑤混合气体的平均摩尔质量不再改变
⑥混合气体的总物质的量不再改变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | N2 | 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2小时时放出的热量为________
②0~1小时内N2的平均反应速率________ mol·L-1·h-1;
③此条件下该反应的化学平衡常数K= ________ (保留两位小数)
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向________ 方向移动(填“正反应”或“逆反应”、“不移动”)。
1.A
2.D
3.A
4.A
5.C
6.B
7.D
8.B
9.B
10.B
11.C
12.C
13.A
14.B
15.C
16.D
17.C
18.BC
19.BD
20.AD
21.ABD
22.I、E AD ABCDE Ⅱ. (1)电流表(1分) 电压表(1分)欧姆表(1分) (2分)(2) ①如图所示(3分,有错不给分) ②ACGHI(2分,少选得1分)
(2分)(2) ①如图所示(3分,有错不给分) ②ACGHI(2分,少选得1分)
23 .(1) a1= = m/s2 =
a2= = m/s2 =
(2)v1= a1?t1=1.6×
(3) H=a1t12+v1t2+a2t22=×1.6×
=
24 .⑴小车经过A点时的临界速度为v1 ,
 (2分),设PQ间距离为L1,
(2分),设PQ间距离为L1, (2分),
(2分),
P到A对小车,由动能定理得 (3分),
(3分),
解得 (2分)
(2分)
(2)设PZ间距离为L2, (2分),
(2分),
小车能安全通过两个圆形轨道的临界条件是在B点时速度为v2,
且在B点时有 (2分),设在P点的初速度为v02,P点到B点的过程,
(2分),设在P点的初速度为v02,P点到B点的过程,
由动能定理得: (3分),
(3分),
 (2分),可知
(2分),可知 <
<
25.(1)设两板间电压为U1时,带电粒子刚好从极板边缘射出电场,则有 (2分),
(2分),
代入数据解得U1=100V(1分)。在电压低于100V时,带电粒子才能从两板间射出,电压高于100V时,带电粒子打在极板上,不能从两板间射出。粒子刚好从极板边缘射出电场时,速度最 大,设最大速度为v1,则有
大,设最大速度为v1,则有 (3分),代入数据解得
(3分),代入数据解得 (1分)(2)设粒子进入磁场时速度方向与OO'的夹角为θ,则速度大小
(1分)(2)设粒子进入磁场时速度方向与OO'的夹角为θ,则速度大小 (2分),粒子在磁场中做圆周运动的轨道半径
(2分),粒子在磁场中做圆周运动的轨道半径 (2分),粒子从磁场中飞出的位置与进入磁场的位置之间的距离
(2分),粒子从磁场中飞出的位置与进入磁场的位置之间的距离 (2分),代入数据解得s=
(2分),代入数据解得s= 逆时针方向做匀速圆周运动。粒子飞出电场时的速度方向与OO'的最大夹角为α ,
逆时针方向做匀速圆周运动。粒子飞出电场时的速度方向与OO'的最大夹角为α , ,α=45°(2分)。当粒子从下板边缘飞出电场再进入磁场时,在磁场中运动时间最长,
,α=45°(2分)。当粒子从下板边缘飞出电场再进入磁场时,在磁场中运动时间最长, (2分);当粒子从上板边缘飞出电场再进入磁场时,在磁场中运动时间最短,
(2分);当粒子从上板边缘飞出电场再进入磁场时,在磁场中运动时间最短, (2分)
(2分)
26、(1)丙的电子式H:C C: H(2分) 离子键、非极性共价键(2分)
(2)高(2分) 水分子间存在氢键而H2S分子中不存在氢键(2分)
(3)1.204×1023(2分)
(4)C2H2(g)+ O2(g)→H2O(l)+2CO2(g);△H=-1294.8kJ?mol―1(4分)
O2(g)→H2O(l)+2CO2(g);△H=-1294.8kJ?mol―1(4分)
(5) 阳极: Fe -2e- = Fe2+ ; 阴极: 2H+ + 2e- = H2 ↑ (2分)
27 (1) 能 (2分)
(2)0.5mol.L-1S-1 (2分)
(3 ) 50% ;1/3 (各2分)
(4) ②④ (2分)
28、(1)Mn2++ClO-+H2O=MnO2↓+2H++Cl-(3分)
促进Al3+、Fe3+水解及Mn2+氧化成MnO2(2分) (2)Fe(OH)3(1分) Al(OH)3(1分)
(3)取过滤II后的滤液1~2 ml于试管中,加入少量KSCN溶液,如果溶液不显红色,证明滤液中无Fe3+(4分)
(4分)CaSO4?2H2O或CaSO4(2分) 以防MgSO4在温度低时结晶析出。(2分)
29、(1) C4H10O (2分) CH2 ==CHCH2CH2―OH (2分)
(2) 加成 取成 (2分)
(3) a;b;c (3分)
(4)D和E: (2分)
(2分)
(5)


 ((3分)
((3分)
或 +
+
 +
+
(6)


 (3分)
(3分)
30(I)、答案:(1)转录和翻译 (2)基因突变 甲患者家族中,部分儿童(如甲患者)从双亲的一方中遗传了基因a,体细胞中只有一个正常基因A,只要一次突变就可能癌变患病,因此患病率明显升高。正常人群中,儿童体细胞内两条13号染色体均有基因A,必须两个基因同时发生突变才会癌变患病,因此发病率很低。(意思接近即可得分)
(3)(父方或母方都可以) 形成生殖细胞的减数第一次分裂间期(DNA复制) 体细胞有丝分裂的间期(DNA复制) 基因诊断
30(II)、答案:(1)主要能源物质 糖或糖类和脂肪
(2)①识别 内吞或胞吞
②流动 融合
③调节能力 胆固醇摄入过多或编码LDL受体蛋白的基因有缺陷(合理给分)
31、答案:⑴在适宜条件下叶圆片进行光合作用,释放的O2多于有氧呼吸消耗的O2,叶细胞间隙中的O2增加,使叶圆片浮力增大
⑵蒸馏水中缺乏C O2和O2,叶圆片不能光合作用和有氧呼吸,其浮力基本不变
⑶①取相同重量、相同生长状况的爬山虎和石榴的新鲜叶片,置于密闭的透明玻璃容器中,在相同适宜光照、温度等条件下测定其各自的C O2吸收速率(或者O2的释放速率),并进行比较(或者其它合理答案)
②取两种植物的叶片做成切片,在显微镜下观察其各自叶横切面,比较两者叶细胞间隙的大小
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com