
题目列表(包括答案和解析)
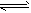 COCl2(g)。某小组同学将不同量的CO和Cl2分别通入体积为2L的恒容密闭容器中进行上述反应,得到如下数据:
COCl2(g)。某小组同学将不同量的CO和Cl2分别通入体积为2L的恒容密闭容器中进行上述反应,得到如下数据: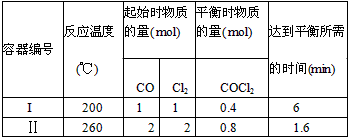
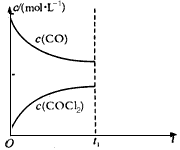

(一)(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图3—2所示的游码尺上画出游码的位置(画“|”表示)。
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 |

(2)图3—3表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是__________mL。
(3)配制![]() 的硫酸溶液200mL所需的玻璃仪器为___________。
的硫酸溶液200mL所需的玻璃仪器为___________。
(二)随着科学技术的发展,阿伏加德罗常数的测定手段越来越多,测定的精确度也越来越高。现有一种简单可行的测定的方法,具体步骤为:
(1)将固体NaCl细粒干燥后,准确称取mg NaCl固体并转移到定容仪器A中;
(2)用滴定管向A仪器中加苯,不断振荡,继续加苯至A仪器的刻度,计算出NaCl固体的体积![]() 。
。
请回答下列问题:
①步骤(1)中A仪器最好使用___________。(填序号)
A.量筒 B.烧杯 C.容量瓶 D.试管
②步骤(2)中用酸式滴定管还是用碱式滴定管______________,理由是_____________。
③能否用水代替苯__________,理由是____________。
④已知NaCl晶体中,靠得最近的![]() 与
与![]() 间的平均距离为a cm(如图3—4),用上述测定方法测得的阿伏加德罗常数
间的平均距离为a cm(如图3—4),用上述测定方法测得的阿伏加德罗常数![]() 的表达式为_______________。
的表达式为_______________。

(三)在配制物质的量浓度溶液时,下列操作出现的后果是(填:“溶液浓度不准确”、“偏低”、“偏高”、“无影响”):
(1)配制氢氧化钠溶液时,称取已吸潮的氢氧化钠固体。_____________。
(2)配制氢氧化钠溶液时,溶液不能澄清,溶质少量不溶解。____________。
(3)配制氯化钠溶液时,容量瓶中有少量水。______________。
(4)定容时,液面上方与刻度相齐时,停止加水。__________。
(5)配制好溶液后,容量瓶未塞好,洒出一些溶液。_____________。
(6)发现溶液液面超过刻度线,用吸管吸出少量水,使液面降至刻度线________________。
(12分)(1)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图3—2所示的游码尺上画出游码的位置(画“|”表示)。
|
砝码质量/g |
50 |
20 |
20 |
10 |
5 |
|
取用砝码情况 |
|
|
|
|
|
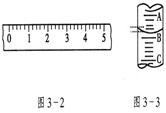
(2)图3—3表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是__________mL。
(3)用18mol?L—1的硫酸溶液配制0.5mol?L—1的硫酸溶液250mL所需的玻璃仪器为___________。
(17分)某学生用托盘天平称量一个小烧杯的质量,如小烧杯的质量为32.6g,用“↓”表示在托盘上放砝码,“↑”表示从托盘上取砝码,请用箭头在下表中填空,表示称量过程,并在图3—2所示的游码尺上画出游码的位置(画“|”表示)。
| 砝码质量/g | 50 | 20 | 20 | 10 | 5 |
| 取用砝码情况 |
|
|
|
|
|
(2)图3—3表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL,如果刻度A为4,量筒中的液体的体积是__________mL。
(3)配制的硫酸溶液200mL所需的玻璃仪器为___________。
1.(16分)
(1)①洗去油污(1分);③在②的滤液中加入稍过量的洗涤过的废铁屑,充分反应后过滤(1分);④将③的滤渣溶入足量的稀硫酸中,过滤,滤液保留待用(1分);(2)⑤、③(1分),将溶液加热到
(3)否(1分),普通自来水中含Cl―,使Ag+被沉淀(1分)。 (共2分)
(4)Fe+2Ag+
Fe2++2Ag,Fe2O3+6H+ 2Fe3++3H2O,Fe+2Fe3+ 3Fe2+,
Fe+2H+ Fe2++H2↑
(各1分,共4分)
(5)抑制Fe2+的水解,防止Fe2+被氧化 (2分)
2.(10分)(1)MnO2, NaOH溶液 (各1分) (共2分)
(2)2NaOH+Cl2==== NaCl+NaClO+H2O (2分)
(3)①不能(1分),HCl气体进入C中,消耗NaOH, 降低NaClO的纯度。(2分)(共3分)
|