
题目列表(包括答案和解析)
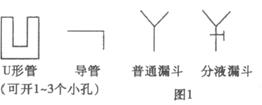
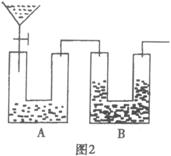
某同学用图2测定Na2CO3试样的纯度(杂质不与水反应),其中A容器中盛有Na2CO3样品10.0g,分液漏斗内盛有稀硫酸,B容器内为碱石灰固体。他利用碱石灰的增重求出纯净的Na2CO3质量,再求纯度。他重复正确操作了三次,结果数据出现了较大偏差(设原容器中CO2气体的含量可忽略不计,各容器内反应完全,下同)
(1)请你分析出现较大偏差的原因__________________________________________________。
通过仔细分析,该同学重新设计了一套实验装置(见图3)。(实验室中可供选择的试剂和药品还有Zn片、浓硫酸、NaOH溶液、CaCO3固体、蒸馏水)

(2)该同学新设计的装置仍不完整,应在_________处(填B或D)添加_________(写出装置及药品的名称)。
(3)A装置中分液漏斗所盛液体为_________,F装置在整套装置中的作用是_______________
_____________________________________________________________________。
(4)如果B、D内不设计任何装置而直接连通A、C、E,则实验结果将_________(填偏高、偏低、无影响)。
| |||||||||||||||
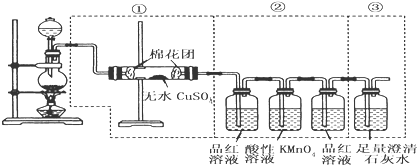
(10分)下图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物。填写下列空白。(已知二氧化硫能和酸性高锰酸钾溶液发生氧化还原反应。)
(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式 。
(2)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,不能检出的物质是____ _。
(3)如果将仪器的连接顺序变为①、③、②,则不能检出的物质是_ _ _和 ,。
(4)如果将第②部分仪器中连接在酸性KMnO4溶液后的装有品红溶液的洗气瓶去掉,则对所作出的结论会有什么影响?
请说明具体原因 。
(10分)下图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物。填写下列空白。(已知二氧化硫能和酸性高锰酸钾溶液发生氧化还原反应。)
(1)写出浓硫酸与木炭粉在加热条件下反应的化学方程式 。
(2)如果将装置中①、②、③三部分仪器的连接顺序变为②、①、③,不能检出的物质是____ _。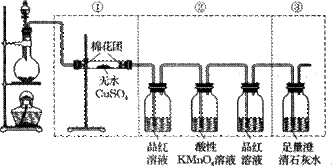
(3)如果将仪器的连接顺序变为①、③、②,则不能检出的物质是_ _ _和 ,。
(4)如果将第②部分仪器中连接在酸性KMnO4溶液后的装有品红溶液的洗气瓶去掉,则对所作出的结论会有什么影响?
请说明具体原因 。
一、选择题
题号
1
2
3
4
5
6
7
8
9
10
答案
C
B
D
D
C
D
C
C
B
B
二、选择题
题号
11
12
13
14
15
16
17
18
19
20
答案
D
A
D
C
D
B
D
D
A
C
三、选择题
题号
21
22
23
24
25
26
27
28
29
30
答案
BC
BD
BD
D
B
C
C
A
BC
BD
题号
31
32
33
34
答案
BC
B
AB
D
 四、填空、简答和计算
四、填空、简答和计算
 35. (1)
(2)
35. (1)
(2)
 |
(3)
(4)BaCO3+2H+==Ba2++CO2↑+H2O
 |
 (5)Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O
(5)Cu+2H2SO4(浓)===CuSO4+SO2↑+2H2O
36.(1)Li 原子失去一个电子后, Li+已经形成了稳定结构,此时再失去电子很困难。
(2) C ;(3) ⅢA族,失去第四个电子时所需能量远远大于失去前三个电子所需能量 。
37.(1)产生白色沉淀,试液变成红色;因为在水中SO2和Cl2反应生成盐酸和硫酸,使石蕊试液变红色,硫酸与BaCl2溶液反应产生BaSO4 沉淀。 (2)③、SO3;②、HCl;①、SO2;③、H2O。
38.(14分)(1)碳、氧、钠、硫(2)CO2+2OH-=H2O+CO32-
(3)
 。
。
39.⑴SiO2 Na2SiO3 H2SiO3
⑵

40.(1)
含有SO 或SO
或SO 中的一种或两种都有。
中的一种或两种都有。
(2) BaCO3;(3)
Br-、S2-
; HCO (除SO
(除SO 或SO
或SO 以外)
以外)
41.(1)Al;H2 ;Cl2(2)非金属;
(3)氧化物或氢化物;SiO2+ Si+2CO↑或O2+H2S
Si+2CO↑或O2+H2S 2H2O+S(其它合理答案均可)
2H2O+S(其它合理答案均可)
42.(1) 、
、 ;
; (2)
(2) ;
; 、
、 (3)
(3) 、
、 ;
;
43.解: 0.5molY的离子得到6.02×1023个电子(即1mol电子)被还原为中性原子,所以1molY应得到2mol电子还原为中性原子,即Y离子应带2个带电荷,则其氧化物的化学式应为YO。
YO + 2HCl=YCl2+H2O
(Y+16)g 2mol
∴ =
=
∴Y=24
又∵Y核中质子数等于中子数,∴Y的质子数为12,应是Mg,位于第三周期ⅡA族。
MgO+2H+=Mg2++H2O
44.解:
由方程式可知: =n(被还原的
=n(被还原的 )
)


45. (1)a≤2/3;(2)a≥2; (3) 2/3<a<2, (1?a/2)mol
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com