
题目列表(包括答案和解析)
| ||
. |
| ||
. |
| ||
| ||


 存在于煤焦油中,所有原子均处于同一平面内,则1mol E 最多能和
存在于煤焦油中,所有原子均处于同一平面内,则1mol E 最多能和

A.B.C.D.E是中学化学常见单质,构成它们的元素的原子序数分别为α、b. c.d.е;且3 (a+b) = 2 (a+c) = 3 (d-a);X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(图中反应物和产物中的H2O已略去):
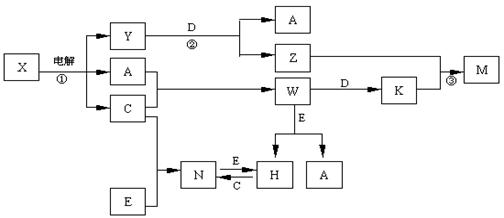
(1)Y的电子式为 ,构成D单质的元素在周期表中位于 周期 族。
(2)反应③的离子方程式为 E的氧化物与D在一定条件下反应的化学方程式为: 。
(3)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断
N为 型晶体。
(4)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为 。
一、选择题:1.B 2.D 3.A 4.A 5.B 6.C 7.B 8.A 9.D 10.C
二、选择题:11.B 12.BD 13.CD 14.BD 15.A 16.BD
三、填空、简答和计算
18.(1)0.045mol/L; (2)35.6, 0.045mol/l
19.小于。设98%H2SO4溶液的密度为d1,浓度为C1;49%H2SO4密度为d2,浓度为C2。分别将质量分数转化为物质的量浓度,可得关系C1=10d1, C2=5d2,则C1:C2=2 d1/d2,由于硫酸溶液浓度越大密度越大,所以C1/C2>2,即C2< C1/2=9.2mol/L.
20.(1)2.1,250,量筒、烧杯、玻璃棒、胶头滴管。(2)B、C、A、F、E、D(3)保证溶质全部转入容量瓶。容量瓶盛放热溶液时,体积不准。(4)浓度偏低;偏低;偏高。(5)宣告实验失败,洗净容量瓶后重新配制;宣告实验失败,洗净容量瓶后重新配制。
21.解:设所加硫酸溶液中含有1molH2SO4,则加入氯化钡溶液中产生BaSO4的物质的量也为1mol,质量为
硫酸的质量分数= ×100%=42.06%
×100%=42.06%
硫酸的物质的量的浓度= =5.49(摩/升)
=5.49(摩/升)
答:该硫酸溶液的质量分数是42.06%,物质的量浓度为5.49摩/升。
22.解:
其体积在标准状况下为12.0mol×
 -12.0 mol×
-12.0 mol×
其体积为
 =
= =378
=378
1体积水吸收378体积NH 气(标准状况)
气(标准状况)
若直接列出总式,同样给分:
 =
= =378
=378
答:标准状况,1体积水吸收了378体积NH 气
气
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com