已知pH为4-5的条件下,Cu
2+几乎不水解,而Fe
3+几乎完全水解.某学生用电解纯净的CuSO
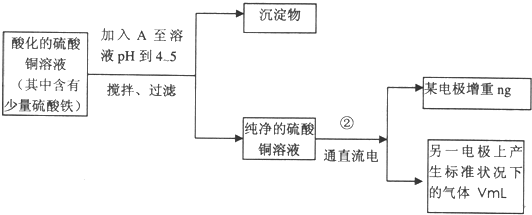
4溶液的方法,并根据电极上析出Cu的质量(n)以及电极上产生气体的体积(V mL 标准状况)来测定Cu的相对原子质量,过程如图1:
回答下列问题:
(1)加入CuO的作用是
消耗H+而调整溶液的pH使之升高,使Fe3+完全水解形成Fe(OH)3沉淀而除去
消耗H+而调整溶液的pH使之升高,使Fe3+完全水解形成Fe(OH)3沉淀而除去
.
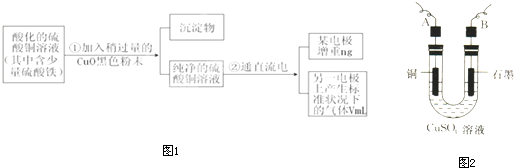
(2)步骤②中所用的部分仪器如图2所示,则A、B分别连直流电源的
负
负
和
正
正
极(填“正”或“负”).
(3)电解开始后,在U形管中可以观察到的现象有:
铜棒变粗,石墨极上有气泡生成,溶液的颜色变浅
铜棒变粗,石墨极上有气泡生成,溶液的颜色变浅
.电解的离子方程式为
.
(4)下列实验操作中必要的是
abde
abde
(填写字母).
a.电解前的电极的质量;b.电解后,电极在烘干称量前,必须用蒸馏水冲洗;c.刮下电解后电极上析出的铜,并清洗,称量;d.电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行;e.在有空气存在的情况下,烘干电极必须用低温烘干的方法.
(5)铜的相对原子质量为
(用带有n、V的计算式表示).