
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
“—÷™£∫Ω´KI°¢—ŒÀ·°¢ ‘º¡X∫ÕµÌ∑€Àƒ÷÷»Ð“∫ªÏ∫œ£¨ŒÞ∑¥”¶∑¢…˙°£
¢ŸœÚ∆‰÷–µŒº”À´—ıÀÆ£¨∑¢…˙∑¥”¶£∫H2O2+2H++2I°• =2H2O+I2£ª
¢⁄…˙≥…µƒI2¡¢º¥”Î ‘º¡X∑¥”¶£¨µ± ‘º¡Xœ˚∫ƒÕÍ∫Û£¨…˙≥…µƒ I2 ≤≈ª·”ˆµÌ∑€±‰¿∂“Ú¥À£¨∏˘æ𠑺¡Xµƒ¡ø°¢µŒ»ÎÀ´—ıÀÆ÷¡»Ð“∫±‰¿∂À˘–˵ƒ ±º‰£¨º¥ø…Õ∆À„£∫H2O2+2H++2I°• = 2H2O+I2µƒ∑¥”¶ÀŸ¬ °£
œ¬±ÌŒ™ƒ≥Õ¨—ß“¿æð…œ ˆ‘≠¿Ì…˺∆µƒ µ—Ⱥ∞ µ—Ⱥ«¬º£®∏˜ µ—Èæ˘‘⁄ “Œ¬Ãıº˛œ¬Ω¯––£©£∫
|
±ý∫≈ |
Õ˘…’±≠÷–º”»Îµƒ ‘º¡º∞∆‰”√¡ø£®mL£© |
¥þªØº¡ |
ø™ º±‰¿∂ ±º‰£®min£© |
||||
|
0£Æ1 mol°§L°•1 KI»Ð“∫ |
H2O |
0£Æ01 mol°§L°•1 X »Ð“∫ |
0£Æ1mol°§L°•1 À´—ıÀÆ |
1 mol°§L1 œ°—ŒÀ· |
|||
|
1 |
20£Æ0 |
10£Æ0 |
10£Æ0 |
20£Æ0 |
20£Æ0 |
ŒÞ |
1£Æ4 |
|
2 |
20£Æ0 |
m |
10£Æ0 |
10£Æ0 |
n |
ŒÞ |
2£Æ8 |
|
3 |
10£Æ0 |
20£Æ0 |
10£Æ0 |
20£Æ0 |
20£Æ0 |
ŒÞ |
2£Æ8 |
|
4 |
20£Æ0 |
10£Æ0 |
10£Æ0 |
20£Æ0 |
20£Æ0 |
5µŒFe2(SO4)3 |
0£Æ6 |
£®1£©“—÷™£∫ µ—È1°¢2µƒƒøµƒ «ÃΩæøH2O2≈®∂»∂‘H2O2+2H++2I°• = 2H2O+I2∑¥”¶ÀŸ¬ µƒ”∞œÏ°£ µ—È2÷–m= £¨n= °£
£®2£©“—÷™£¨I2”ÎXÕÍ»´∑¥”¶ ±£¨¡Ω’þŒÔ÷ µƒ¡ø÷Ʊ»Œ™1°√2°£∞¥±Ì∏Ò÷–µƒX∫ÕKIµƒº”»Î¡ø£¨º”»ÎV£®H2O2£©>________£¨≤≈»∑±£ø¥µΩ¿∂…´°£
£®3£© µ—È1£¨≈®∂»c(X)°´ tµƒ±‰ªØ«˙œþ»ÁÕº£¨»Ù±£≥÷∆‰À¸Ãıº˛≤ª±‰£¨«Î‘⁄¥Ã‚ø®◊¯±ÍÕº÷–£¨∑÷±ª≠≥ˆ µ—È3°¢ µ—È4£¨c(X) °´ tµƒ±‰ªØ«˙œþÕº£®Ω¯––œý”¶µƒ±Í◊¢£©°£

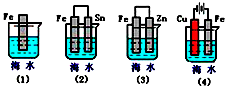
£®4£© µ—È4±Ì√˜£∫¡ÚÀ·Ã˙ƒÐ÷∏þ∑¥”¶ÀŸ¬ °£¥þªØº¡ƒÐº”øÏ∑¥”¶ÀŸ¬ «“ÚŒ™¥þªØº¡ (ÃÓ°∞÷∏þ°±ªÚ°∞ΩµµÕ°±)¡À∑¥”¶ªÓªØƒÐ°£
£®5£©ª∑æ≥”—∫√–Õ¬¡°™µ‚µÁ≥ÿ“——–÷∆≥…𶣨“—÷™µÁ≥ÿ◊Ð∑¥”¶Œ™£∫2Al(s)+3I2(s) 2AlI3(s)°£∫¨I°•¥´µº”–ª˙æßÃÂ∫œ≥…ŒÔ◊˜Œ™µÁΩ‚÷ £¨∏√µÁ≥ÿ∏∫º´µƒµÁº´∑¥”¶Œ™£∫________________________£¨≥‰µÁ ±Al¡¨Ω”µÁ‘¥µƒ___________º´°£
2AlI3(s)°£∫¨I°•¥´µº”–ª˙æßÃÂ∫œ≥…ŒÔ◊˜Œ™µÁΩ‚÷ £¨∏√µÁ≥ÿ∏∫º´µƒµÁº´∑¥”¶Œ™£∫________________________£¨≥‰µÁ ±Al¡¨Ω”µÁ‘¥µƒ___________º´°£
£®6£©“—÷™£∫N2H4(l) +2H2O2(l)= N2(g)+4H2O(g) °˜H1= £≠640kJ/mol
H2O£®l£©=H2O£®g£© °˜H2£Ω+44.0kJ/mol
‘Ú0.25mol “∫èά”Γ∫èÀ´—ıÀÆ∑¥”¶…˙≥…“∫èÀÆ ±∑≈≥ˆµƒ»»¡ø « °£



| ||
| °˜ |
| ||
| °˜ |
| ||
| °˜ |
| ||
| °˜ |
| 1 |
| 2 |
| 1 | 2 |
| 1 |
| 2 |
| Œ¬∂»£®°Ê£© | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| Õ≠∆Ωæ˘»ÐΩ‚ÀŸ¬ £®°¡10-3mol?L-1?min-1£© |
7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
 –¥≥ˆœ¬¡–∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã Ω£Æ
–¥≥ˆœ¬¡–∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã Ω£Æ1.A(µ‚µ•÷ ”ˆµÌ∑€±‰¿∂…´£¨∂¯≤ª «µ‚À·ºÿ)
2.D(Õ¨Œ¬Õ¨—πœ¬£¨mg∆¯ÃÂA”Îng∆¯ÃÂBµƒ∑÷◊” ˝ƒøœýÕ¨£¨Àµ√˜ŒÔ÷ µƒ¡øœýÕ¨£¨A°¢B°¢C’˝»∑£¨DÕ¨Œ¬Õ¨—πœ¬£¨∆¯ÃÂA”Î∆¯ÃÂBµƒ√Ð∂»÷Ʊ»µ»”⁄À¸√«µƒŒÔ÷ µƒ¡ø÷Ʊ»Œ™m £∫ n)
3.C(¥”¢€¥¶µº≥ˆµƒ∆¯ÃÂ∫¨”–…Ÿ¡øSO2°¢O2 °¢N2µ»£¨≤ªø…÷±Ω”≈≈»Î¥Û∆¯£¨∑Ò‘Ú‘Ï≥…Œ€»æ)
4.A(BœÓ”…”⁄≤ª÷™µ¿∆¯Ãµƒ◊¥Ã¨£¨
5.A(∑≈≥ˆ»»¡ø¶§H<0£¨À˘“‘A¥ÌŒÛ£ª∆‰À¸Àµ∑®æ˘’˝»∑)
6.A(ÀƵƒ»»Œ»∂®–‘±»Ωœ∏þ «“ÚŒ™ÀÆ∑÷◊”÷–«‚—ıº¸µƒº¸ƒÐ¥Û£ªΩ ÙæßõºµÁ «“ÚŒ™∫¨”–◊‘”…“∆∂صƒµÁ◊”£ª¿Î◊”æßÔ≤∂»Ωœ¥Û°¢ƒ—”⁄—πÀı «“ÚŒ™¿Î◊”º¸º¸ƒÐ¥Û)
7.D (D÷–…œœ¬“∆∂Ø ±£¨¡Ω∂À“∫√Ê º÷’∆Ω∫‚Àµ√˜◊∞÷√¬©∆¯)
8.B(π˝—ıªØƒ∆πÃÔÎÀÆ∑¥”¶£¨ «∑≈»»∑¥”¶£¨A°¢C¥ÌŒÛ£ª∑≈»» ππ„ø⁄∆ø÷–∆¯ÃÂŒ¬∂»…˝∏þ≈Ú’Õ£¨‘Ú”“±þ…˝∏þ◊Û±þœ¬Ωµ)
9.A(ClO£≠£´2I£≠£´2H£´===Cl£≠£´I2£´H2O£ªSO£´I2£´H2O===2I£≠£´SO£´2H£´£¨À˘“‘ø…÷™—ıªØ–‘Œ™£∫ClO£≠>I2>SO£¨“ÚŒ™¢⁄÷–º”»Îπ˝¡øµƒNa2SO3 »Ð“∫£¨À˘“‘¢€÷–∫¨”–BaSO3≥¡µÌ£ª¢Ÿ÷–¡ÚÀ·÷ª∆µΩÀ·–‘◊˜”√£¨¢⁄÷ªƒÐ÷§√˜SO”–ªπ‘≠–‘)
10.C(∂˛‘™»ıÀ·”¶∑÷≤ΩµÁ¿Î£ª≤ðÀ·µŒ∂®KMnO4 Ù”⁄—ıªØªπ‘≠µŒ∂®£¨≤ª”√÷∏ 溡£ª““∂˛À·Õ—ÀÆ∑÷Ω‚≤˙ŒÔ «CO°¢CO2∫ÕH2O)
11.A((NH4)2SO4∫ÕCH3COOH√˜œ‘ Ù”⁄µÁΩ‚÷ £ªCl2 «µ•÷ º»≤ª Ù”⁄µÁΩ‚÷ “≤≤ª Ù”⁄∑«µÁΩ‚÷ £ªÀ‰»ªNH3µƒÀƻГ∫ƒÐπªµºµÁ£¨ƒ« «”…”⁄…˙≥…¡À“ªÀÆ∫œ∞±µƒ‘≠“Ú£¨π NH3 Ù”⁄∑«µÁΩ‚÷ °£)
12.D(CsCl∫ÕNaClµƒ“ı°¢—Ù¿Î◊”≈≈¡–∑Ω Ω≤ªÕ¨£ªΩ ÙæßÃÂ÷–÷ª”–—Ù¿Î◊”£¨√ª”–“ı¿Î◊”£ª∑÷◊”æßÃÂ÷–≤ª“ª∂®∫¨”–π≤º€º¸»Áœ°”–∆¯ÃÂ)
13.D(¢ŸÀµ√˜”–Br£≠°¢CO£¨”–COæÕ√ª”–Fe2£´¢⁄Àµ√˜√ª”–SO¢€Àµ√˜√ª”–I£≠)
14.D(ƒÐ∑¢…˙’‚¡Ω∏ˆµÁº´∑¥”¶µƒø…ƒÐ «‘≠µÁ≥ÿ£¨“≤ø…ƒÐ «µÁΩ‚≥ÿ£¨»Áπ˚ «‘≠µÁ≥ÿ£¨‘ÚbŒ™Ã˙µÁº´£¨aŒ™√ªÃ˙ªÓ∆√µƒΩ ÙªÚ∑«Ω Ù◊ˆµÁº´£¨µÁΩ‚»Ð“∫Œ™∫¨Õ≠¿Î◊”µƒ»Ð“∫£ª»Áπ˚ «µÁΩ‚≥ÿ£¨b”√Ã˙◊ˆµÁº´∫ÕµÁ‘¥µƒ’˝º´œý¡¨£¨aø…“‘∫ÕÃ˙œýÕ¨µƒµÁº´“≤ø…“‘≤ªÕ¨£¨»Ð“∫Œ™∫¨Õ≠¿Î◊”µƒ»Ð“∫)
15.C(A≥∆¡ø ±”¶◊یԔ“¬Î£¨B≈‰÷∆150mL0.10mol/L»Ð“∫”¶”√150mLµƒ»ð¡ø∆ø£¨∂¯«““™”√≤£¡ß∞Ù“˝¡˜£ªD¿‰ƒ˝ÀƵƒ∑ΩœÚ”¶¥”œ¬Ω¯…œ≥ˆ)
16.D(¢ŸÀ˘»°≈®¡ÚÀ·µƒÃª˝…Ÿ£¨¢⁄¢€¢Ðæ˘‘Ï≥…»Ð÷ µƒÀ ß)
17.Œ Â1£∫(1)∫œ≥…∞±π§“µ°°¡ÚÀ·π§“µ(∆‰À˚∫œ¿Ì¥∞∏“≤’˝»∑) (2∑÷)
Œ Â2£∫Cu£´4H£´£´2NO(≈®)===Cu2£´£´2NO2°¸£´2H2O
3Cu£´8H£´£´2NO(œ°)===3Cu2£´£´2NO°¸£´4H2O(∆‰À˚∫œ¿Ì¥∞∏“≤’˝»∑)(2∑÷)
ªØ—ß?µ⁄“≥(º˚∑¥√Ê)Œ Â3£∫∑≈»»°°C(Ω∏’ Ø°¢s)£ΩC( ؃´°¢s)£ª¶§H£Ω£≠1.90kJ/mol(2∑÷)
Œ Â4£∫(1)µ⁄∂˛∏ˆ∑¥”¶Œ™£∫Al3£´£´3OH£≠===Al(OH)3°˝ (2∑÷)
(2)◊Ó∫Û“ª∏ˆ¿Î◊”∑¥”¶Œ™£∫Al(OH)3£´OH£≠===AlO£´2H2O (2∑÷)
Œ Â5£∫4KMnO4£´5KI£´7H2SO4===4MnSO4£´I2£´3KIO3£´3K2SO4£´7H2O (2∑÷) (∆‰À˚∫œ¿Ì¥∞∏“≤’˝»∑)
18.(1)¢Ÿ2Cl£≠£≠2e£≠£ΩCl2°¸(2∑÷)°°”√ ™»ÛµƒµÌ∑€£≠KI ‘÷ΩøøΩ¸Yº´÷ßπÐø⁄(∆‰À¸∫œ¿Ì¥∞∏æ˘ø…)(2∑÷)
¢⁄”…”⁄2H£´£´2e£≠£ΩH2°¸°°∑≈≥ˆ«‚∆¯£¨ πÀƵƒµÁ¿Î∆Ω∫‚œÚ’˝∑¥”¶∑ΩœÚ“∆∂Ø£¨ πc(OH£≠)≤ª∂œ‘ˆ¥Û£¨À˘“‘pHª·‘ˆ¥Û(2∑÷)
¢€œ»”–∞◊…´≥¡µÌ…˙≥…£¨ºÃ∂¯±‰≥…ª“¬Ã…´£¨◊Ó∫Û±‰≥…∫Ï∫÷…´(2∑÷)
(2)¢ŸA(1∑÷)°°¢⁄B(1∑÷)
19.(√øø’2∑÷)(1)NaI°°NaClO
(2)2I£≠£´ClO£≠£´H2O===I2£´Cl£≠£´2OH£≠°°I2£´5ClO£≠£´2OH£≠===2IO£´5Cl£≠£´H2O
(3)Cl2£´2NaOH===NaClO£´NaCl£´H2O
20.(1)KClO3 (1∑÷)°°H????????H(1∑÷)
(2)¢Ÿπÿ±’∑÷“∫¬©∂∑ªÓ»˚£¨‘⁄II÷–º”ÀÆ£¨√ªπ˝≥§µºπÐø⁄£¨”√æ∆æ´µ∆Œ¢»»‘≤µ◊…’∆ø£¨»ÙII÷–”–∆¯≈ð√∞≥ˆ£¨Õ£÷πº”»»∫Û£¨”–ÀÆΩ¯»ÎII÷–µƒ≥§µºπУ¨–Œ≥…“ª∂ŒŒ»∂®µƒÀÆ÷˘£¨‘Ú÷§√˜I∆¯√Ж‘¡º∫√°£ (ªÚ”√÷πÀƺ–º–◊°c¥¶£¨œÚ∑÷“∫¬©∂∑÷–º”ÀÆ£¨¥Ú∑÷“∫¬©∂∑µƒªÓ»˚£¨»Ù∑÷“∫¬©∂∑÷–µƒÀÆ≤ª‘Ÿœ¬¡˜£¨‘Ú÷§√˜I∆¯√Ж‘¡º∫√°£)(2∑÷)
¢⁄MnO2£´4H£´£´2Cl£≠Mn2£´£´Cl2°¸£´2H2O(2∑÷)
¢€S2£≠£´Cl2===S°˝£´2 Cl£≠(2∑÷)
ªØ—ß?µ⁄“≥ ¢ÐII°°III(1∑÷)°°≥˝»•¬»∆¯÷–µƒÀÆ’Ù∆¯(ªÚ∏…‘Ô¬»∆¯)(1∑÷)
(3)Cl2£´H2O2===2HCl£´O2(2∑÷)
21.(1)7Cl2£´14NaOH===9NaCl£´4NaClO£´NaClO3£´7H2O
(2)C(NaCl)£Ω1.8mol/L£¨Cl(NaClO)£Ω0.8mol/L£¨C(NaClO3)£Ω0.2mol/L°°(√ø∏ˆ2∑÷)
Ω‚Œˆ£∫Ω‚¥¥Àµƒπÿº¸ «µ⁄(1)Œ .ø…∏˘æðµ√ ßµÁ◊” ˝œýµ»»∑∂®…˙≥…ŒÔNaCl°¢NaClO°¢NaClO3µƒŒÔ÷ µƒ¡ø÷Ʊ»£¨Ω¯∂¯»∑∂®ªØ—ß∑Ω≥à Ω÷–ªØ—ߺ∆À„ ˝.
(1)“¿Ã‚“‚ø……Ë…˙≥…NaClOµƒŒÔ÷ µƒ¡øŒ™4mol£¨NaClO3µƒŒÔ÷ µƒ¡øŒ™1mol£¨…Ë…˙≥…NaClµƒŒÔ÷ µƒ¡øx£¨∏˘æðµ√ ßµÁ◊”µƒŒÔ÷ µƒ¡øœýµ»£¨”–£∫1°¡x£Ω1°¡4mol£´5°¡1mol£¨Ω‚µ√£∫x£Ω9mol.
NaCl°¢NaClO°¢NaClO3ªØ—ߺ∆¡ø ˝÷Ʊ»”Î…˙≥…∂‘”¶ŒÔ÷ µƒŒÔ÷ µƒ¡øœýµ»£¨º¥µ»”⁄9°√4°√1.æð¥Àø…–¥≥ˆ◊еƒªØ—ß◊÷∑Ω≥Ã Ω£∫7Cl2£´14NaOH===9NaCl£´4NaClO£´NaClO3£´7H2O
(2)n(Cl2)£Ω
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com