
题目列表(包括答案和解析)
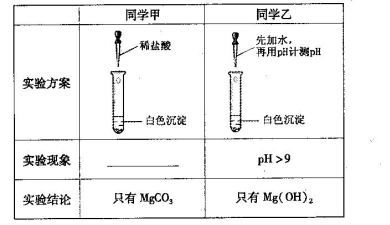
(13分)某研究性学习小组欲探究Na2CO3溶液与MgCl2溶液反应产生白色沉淀的成分,小组成员做如下实验
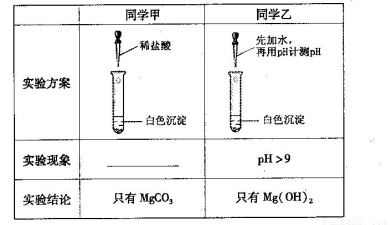
(1)若按所得的结论分析,甲观察到的实验现象是___________________________。
(2)在探究沉淀物成分前,甲、乙都将沉淀物从溶液中分离出来,洗涤并干燥。同学丙认为他们并未将沉淀洗涤干净,请用简单的实验证明丙的观点。
(3)同学丁认为甲结论不合理,理由是Ksp(MgCO3)___Ksp [Mg(OH)2](选填“<”或“>”),所以沉淀物未必是MgCO3。经查阅资料得知:该白色沉淀的组成应为Mgx(OH)y(CO3)z·nH2O。为确定沉
淀物的具体组成,他设计下图装置进行实验(所有夹持装置已省略)。
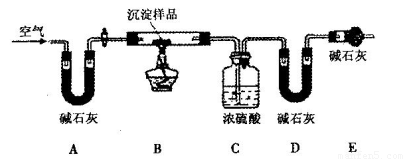
(4)请将丁设计的实验步骤补充完整:
①检查装置气密性;
②先装入药品,并称量相关装置的质量,后连接各装置;
③________________________________________________________;
④停止加热,持续通入空气直至实验结束,再次称量步骤②中相关装置的质量。
(5)装置E中碱石灰的作用是_________________________________________________。
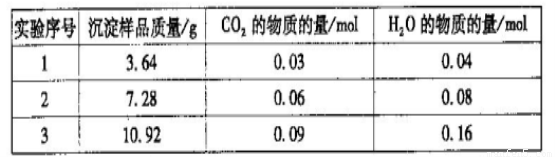
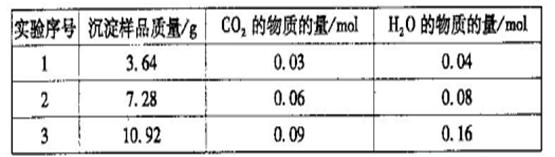
三次实验所得数据如下:(部分数据已换算为相应的物质的量)
 ??
??
(6)分析实验数据可知,第_________组出现误差较大的数据,应舍去。由实验数据计算
得该白色沉淀物的组成为___________(选填序号)。
a.Mg2(OH)2CO3·3H2O?????? b.Mg(OH)2(CO3)2·3H2O
c.Mg4(OH)2(CO3)3·3H2O??? d.Mg5(OH)4(CO3)3·2H2O
(13分)某研究性学习小组欲探究Na2CO3溶液与MgCl2溶液反应产生白色沉淀的成分,小组成员做如下实验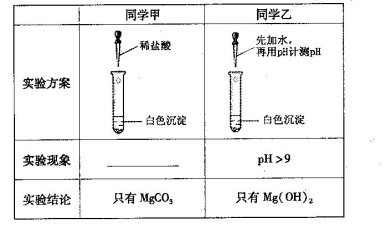
(1)若按所得的结论分析,甲观察到的实验现象是___________________________。
(2)在探究沉淀物成分前,甲、乙都将沉淀物从溶液中分离出来,洗涤并干燥。同学丙认为他们并未将沉淀洗涤干净,请用简单的实验证明丙的观点。
(3)同学丁认为甲结论不合理,理由是Ksp(MgCO3)___Ksp [Mg(OH)2](选填“<”或“>”),所以沉淀物未必是MgCO3。经查阅资料得知:该白色沉淀的组成应为Mgx(OH)y(CO3)z·nH2O。为确定沉
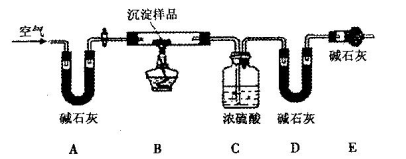
淀物的具体组成,他设计下图装置进行实验(所有夹持装置已省略)。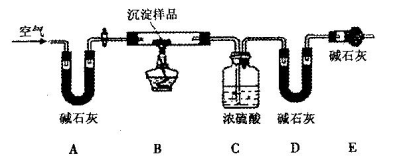
(4)请将丁设计的实验步骤补充完整:
①检查装置气密性;
②先装入药品,并称量相关装置的质量,后连接各装置;
③________________________________________________________;
④停止加热,持续通入空气直至实验结束,再次称量步骤②中相关装置的质量。
(5)装置E中碱石灰的作用是_________________________________________________。
三次实验所得数据如下:(部分数据已换算为相应的物质的量)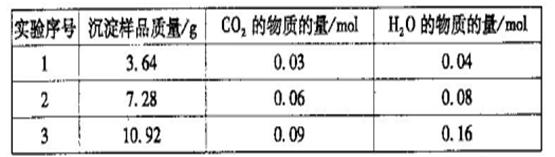
(6)分析实验数据可知,第_________组出现误差较大的数据,应舍去。由实验数据计算
得该白色沉淀物的组成为___________(选填序号)。
a.Mg2(OH)2CO3·3H2O b.Mg(OH)2(CO3)2·3H2O
c.Mg4(OH)2(CO3)3·3H2O d.Mg5(OH)4(CO3)3·2H2O

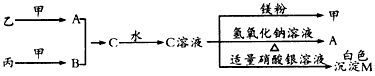
①甲、乙、丙、丁均为短周期元素形成的单质,常温下甲、乙、丙为气体,丁为中学化学中常见的金属单质。
②甲中所含元素的核电荷数是乙、丙所含元素的核电荷数之和。
③丁中所含元素原子的最外层电子数是乙中所含元素原子的最外层电子数的2倍。
④常温下,X是无色液体,Z是刺激性气体,X与W的反应能生成Z及另一种白色沉淀。
试回答:
(1)Y的化学式是______________,丙的电子式为______________。
(2)X与W反应的化学方程式是_______________________________________________。
(3)常温下某Z的水溶液的pH等于11,则该溶液中由水电离产生的OH-的物质的量浓度为______________。
(4)已知
一.选择题(48分)
题号
1
2
3
4
5
6
7
8
答案
A
D
A
C
B
C
B
B
题号
9
10
11
12
13
14
15
16
答案
A
D
C
C
B
B
D
A
二.非选择题(52分)
17.(1) .
. (2)
(2) .
. (3)
(3)
(4) (每空2分,答错或少答1个扣1分,扣到0分为止)
(每空2分,答错或少答1个扣1分,扣到0分为止)
18.(1)验证锂.钠.钾的活泼性(或同一主族,从上到下元素的金属性逐渐增强)(2分);c(1分)
(2)① (各1分)
(各1分)
② (或
(或 (2分)
(2分)
19.(1)第三周期 ⅦA(1分)
(2) 氯碱(2分)
氯碱(2分)

(3)
(4) ;
; KJ/mol(2分)
KJ/mol(2分)
或 ;
; KJ/mol
KJ/mol
(5)离子晶体(1分)
20.(1)硫  离子键.非极性键(4分)
离子键.非极性键(4分)
(2) (2分)
(2分)
(3)① (2分)
(2分)
② (2分)
(2分)
21.(1)
(2)分液漏斗(1分)
(3)饱和食盐水(或饱和氯水)(1分)浓硫酸(1分)
(4) (1分)酒精(汽油.苯等有机溶剂或其他合理答案)(1分)
(1分)酒精(汽油.苯等有机溶剂或其他合理答案)(1分)
(5)使生成的 升华,与其他固体分离(2分)
升华,与其他固体分离(2分)
(6)吸收多余的 ,防止污染空气(1分)
,防止污染空气(1分)
(7)连接 的导管易被
的导管易被 固体堵塞(2分)
固体堵塞(2分)
22.(1)0.16 (2)0.03 0.05 (3)5.72
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com