
题目列表(包括答案和解析)
(11分)短周期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
(1)已知相关物质之间存在如下变化:
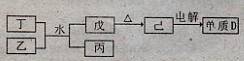
①丁与乙和水反应生成戊和丙的离子方程式为 ,由物质已电解得到单质D的化学方程式为 ;
②0.lmoL/L的丙溶液中所含离子浓度由大到小排列顺序为 。
(2)已知E及其化合物有以下变化:
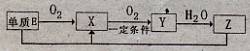
写出单质E与化合物Z在一定条件下反应生成.X和水的化学方程式 。
由A、B、C、D、E5种元素中的.两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为____ (任写一个即可)。
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2L的该无色气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
(11分)短周期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
(1)已知相关物质之间存在如下变化:
①丁与乙和水反应生成戊和丙的离子方程式为 ,由物质已电解得到单质D的化学方程式为 ;
②0.lmoL/L的丙溶液中所含离子浓度由大到小排列顺序为 。
(2)已知E及其化合物有以下变化:
写出单质E与化合物Z在一定条件下反应生成.X和水的化学方程式 。
由A、B、C、D、E5种元素中的.两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为____ (任写一个即可)。
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2L的该无色气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
(11分)短周
 期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
(1)已知相关物质之间存在如下变化: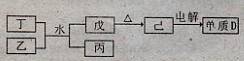
①丁与乙和水反应生成戊和丙的离子方程式为 ,由物质已电解得到单质D的化学方程式为 ;
②0.lmoL/L的丙溶液中所含离子浓度由大到小排列顺序为 。
(2)已知E及其化合物有以下变化: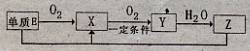
写出单质E与化合物Z在一定条件下反应生成.X和水的化学方程式 。
由A、B、C、D、E5种元素中的.两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为____ (任写一个即可)。
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2L的该无色气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液全吸收后没有气体残留, 所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
短周期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的.
(1)已知相关物质之间存在如下变化:
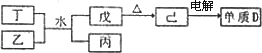
①丁与乙和水反应生成戊和丙的离子方程式为________,由物质已电解得到单质D的化学方程式为________;
②0.1 moL/L的丙溶液中所含离子浓度由大到小排列顺序为________.
(2)已知E及其化合物有以下变化:
写出单质E与化合物Z在一定条件下反应生成.X和水的化学方程式________.
由A、B、C、D、E5种元素中的.两种元素,可形成既含极性键又含非极性键的18电子的分子,该分子的分子式为________(任写一个即可).
(3)C有多种氧化物,其中之一是一种无色气体,在空气中迅速变成红棕色,在一定条件下,2 L的该无色气体与0.5 L的氧气相混合,若该混合气体被足量的NaOH溶液全吸收后没有气体残留,所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是________.

 期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。
期主族元素A、B、C、D、E原子序数依次增大,A元素单质常温常压下是最轻的气体,B元素所形成化合物种类最多,C的最高价氧化物对应水化物甲与其气态氢化物乙能够化合形成盐丙;D元素的离子半径是同周期元素形成的简单离子中最小的。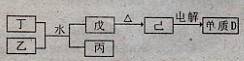
 所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
所生成R的含氧酸盐只有一种,则该含氧酸盐的化学式是 。
16.(1)水 浓硫酸 ;(2)检查气密性,将G弯管浸没在盛有水的烧杯中,温热烧瓶B,观察G管口,若有气泡逸出,说明装置的气密性良好;
(3)先从A瓶逐滴滴加液体, 检验H2的纯度;(4) ,
,  。
。
17.(1) 2Fe3++H2S
= S↓+2Fe2++2H+, Na2S+2H2O S↓+H2↑+2NaOH
S↓+H2↑+2NaOH
或S2-+2H2O S↓+H2↑+2OH-,产物NaOH可循环使用,也可得副产品H2;
S↓+H2↑+2OH-,产物NaOH可循环使用,也可得副产品H2;
(2)阳离子(Na+),钛(或石墨);
(3)4, 正四面体。
18.(1)Al(OH)3+OH---=AlO2-+2H2O ; (2) ;
;
(3)SO2+Cl2+2H2O=H2SO4+2HCl ; (4)HCl>H2S;
(5)S2->Cl ->Na+>Al3+;(6)Cl2O7(l)+H2O(l)=2HClO4(aq);△H=-4QkJ/mol。
19. (1) ①SiHCl3+H2= Si+3HClwww. Ks5 u.com
②3SiHCl3+3H2O===H2SiO3+H2↑+3HCl;高温下,H2遇O2发生爆炸。(2)ABCE
(3)生成白色絮状沉淀,又刺激性气味的气体生成。
20.
(1)NaCl; (2)Cu+2H2SO4 CuSO4+ SO2↑+2H2O,高温、催化剂; (3)CH3CH2OH。
CuSO4+ SO2↑+2H2O,高温、催化剂; (3)CH3CH2OH。
21. ⑴b ; ⑵加热褪色后的溶液,若溶液恢复红色,则原通入气体为SO2,若溶液不变红,则原通入气体是O3 ; ⑶2Fe+3Cl2 2FeCl3 Fe+S
2FeCl3 Fe+S FeS(其他合理答案均给分);
FeS(其他合理答案均给分);
⑷①H-C≡N ; ⑸16w1:(44w2-aw1)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com