
题目列表(包括答案和解析)
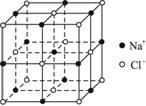
(1)请将其中代表Na+的圆圈用笔涂黑,以完成氯化钠晶体结构示意图并确定晶体的晶胞。
(2)从晶胞中分析氯化钠化学式为NaCl。
(3)在每个Na+周围与它最近的且距离相等的Na+有多少个?
下图为氯化钠晶体结构图,图中直线交点处为NaCl晶体中Na+与Cl-所处的位置(不考虑体积的大小)。
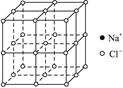
(1)请将其中代表Na+的圆圈用笔涂黑,以完成氯化钠晶体结构示意图并确定晶体的晶胞。
(2)从晶胞中分析氯化钠化学式为NaCl。
(3)在每个Na+周围与它最近的且距离相等的Na+有多少个?
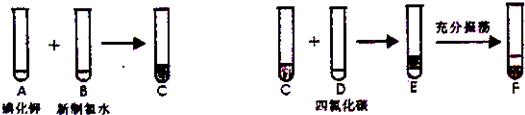
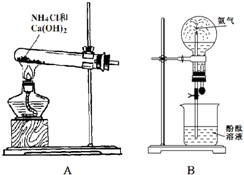 实验是科学探究的重要途径,请将下列有关实验的问题填写完整.
实验是科学探究的重要途径,请将下列有关实验的问题填写完整.
| 1 |
| 2 |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |



湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com