
题目列表(包括答案和解析)
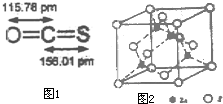 用于合成氨的工业煤气中含有S2H、C2H5SH(乙硫醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理.
用于合成氨的工业煤气中含有S2H、C2H5SH(乙硫醇)、COS(羰基硫)、CS2等含硫化合物,工业上无机硫常用氧化锌法处理,有机硫可用钴钼催化加氢处理.合成氨反应(N2+3H2  2NH3+92.4KJ)在化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。
2NH3+92.4KJ)在化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。

30. X的化学式为 ;X的状态为_______态。
31. 据右图分析,下列说法正确的是 (填写编号)。
a.在此温度下,有利于平衡正向移动,可提高氨的产量
b.铁触媒的使用有利于平衡正向移动
c.工业生产受动力、材料、设备等条件的限制,选择此压强
d.为提高原料的转化率,采用循环操作
32. 常温下氨气极易溶于水,其水溶液可以导电。
① 氨水中水的离子积常数的数值是_______________________;
② 将相同体积、相同物质的量浓度的氨水和盐酸混合后,
溶液中离子浓度由大到小依次为 。
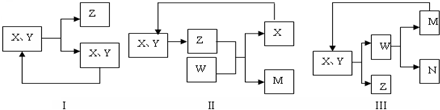
氨有着广泛的用途,可用于化肥、硝酸、合成纤维等工业生产。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应可生成氨气: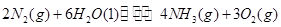
该反应在固定体积的密闭容器中进行,有关说法正确的是_____________(填序号字母)。
A.反应处于平衡状态时,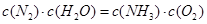 |
B.反应达到平衡后,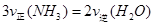 |
| C.体系的总压强不变,说明反应已达平衡 |
| D.混合气体的密度保持不变,说明反应已达平衡 |
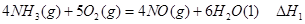 ①
①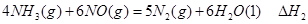 ②
②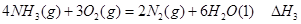 ③
③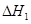 、
、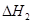 、
、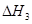 三者之间关系的表达式,
三者之间关系的表达式,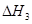 =_________。
=_________。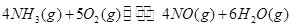
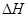 =
=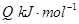


| 时间/浓度 |   | 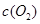  | 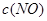  | 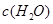  |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | a | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |

A.反应处于平衡状态时, |
B.反应达到平衡后, |
| C.体系的总压强不变,说明反应已达平衡 |
| D.混合气体的密度保持不变,说明反应已达平衡 |
 ①
①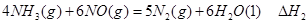 ②
② ③
③ 、
、 、
、 三者之间关系的表达式,
三者之间关系的表达式, =_________。
=_________。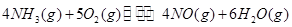
 =
=


| 时间/浓度 |   |   |   |   |
| 起始 | 4.0 | 5.5 | 0 | 0 |
| 第2min | 3.2 | a | 0.8 | 1.2 |
| 第4min | 2.0 | 3.0 | 2.0 | 3.0 |
| 第6min | 2.0 | 3.0 | 2.0 | 3.0 |
15、(12分) (1)Mg2+、Al3+、NO 、SO
、SO (4分)
(4分)
(2)Fe2+、Ba2+、I-、HCO (4分)
(4分)
(3)焰色反应,取少量原溶液,加入Ba(NO3)2溶液后,取上层清液加入AgNO3溶液和稀HNO3(4分)
16、⑴C、D、F、E; ⑵10;⑶浓硫酸,干燥SO2 ⑷A、D ⑸⑤
⑹42%(或0.42);NaCl、Na2SO4
17、I.(1)溶液显色所需要的时间。
(2)①2NO+O2+4CO 4CO2+N2(3分);②-1160 kJ?mol-1;
4CO2+N2(3分);②-1160 kJ?mol-1;
(3)①该研究只能提高化学反应速率,不能使化学平衡发生移动、 D
II.NO2(2)NH4NO3 N2O+2H2O(3分)
N2O+2H2O(3分)
18、 (1) 、
、 、Mg2+(2)氟,2H2O+
、Mg2+(2)氟,2H2O+
(3)  2CO↑+Si (4)2Mg+CO2
2CO↑+Si (4)2Mg+CO2 2MgO+C
2MgO+C
19、Ⅰ.
 Ⅱ.(1)HgCl2 HgCl++Cl―(1分);
Ⅱ.(1)HgCl2 HgCl++Cl―(1分);
2Fe2++2HgCl2=Hg2Cl2↓+2Fe3++2Cl―(2分);
K=[Fe3+]2―[Cl―]2/[Fe2+]2[HgCl2]2(2分)
(2)不能。因为加热能促进氯化铝水解,且氯化氢逸出也使平衡
|