CuO
⑤6CO2
+ 6H2O 光照 叶绿素 C6H12O6
+ 6O2
⑷ D
⑸保持表面洁净、干燥或其它合理方法均可
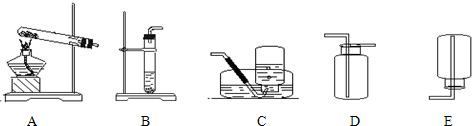
26.(4分) B; A; B; A
27.(7分) ⑵2KMnO4
 K2MnO4 + MnO2
+ O2↑
K2MnO4 + MnO2
+ O2↑
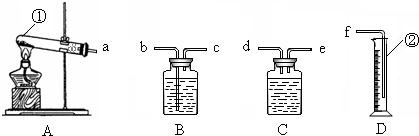
⑶ ①试管 ②量筒 ⑷c→b
⑸ ①试管口没有放棉花 ②集气瓶底没有放少量的水或铺一层细沙
③未冷却到室温就读数
28.(5分) ⑴
方法二
氧化铜
取少量样品分别与氧化铜反应,使氧化铜溶解且溶液由无色变为蓝色,则原样品为稀盐酸,无现象的为氯化钠溶液。
方法三
氢氧化铜
取少量样品分别与氧化铜反应,使氢氧化铜溶解溶解且溶液由无色变为蓝色,则原样品为稀盐酸,无现象的为氯化钠溶液。
其他合理答案均可
⑵用玻璃棒分别沾取两种待测溶液,在酒精灯上灼烧。
29.(10分)⑴除去水分(防止过氧化钠与水反应);B、C;E
⑵ 2Na2O2 + 2CO2 ==
2Na2CO3 + O2
⑶不能;根据质量守恒定律,反应物中不含H元素(答出原因才给分)
⑷吸收多余的二氧化碳(防止二氧化碳对检验氧气产生干扰);
实验方案
实验
现象
有关化学方程式
实验结论
①取样,先向溶液中滴加过量的 CaCl2或BaCl2或Ca(NO3)2 或Ba(NO3)2 溶液;
产生
白色
沉淀
CaCl2+ Na2CO3 == CaCO3↓+2 NaCl
D溶液中有NaOH剩余。
②静置,取上层清液,滴加CuCl2或Cu(NO3)2或CuSO4 溶液。
产生蓝色沉淀
2NaOH+CuCl2== Cu (OH)2↓
+2 NaCl
四、(6分)
 30.解:⑴设参加反应的氯化钠的质量为x,生成氢气、氢氧化钠的质量分别为y、z。
30.解:⑴设参加反应的氯化钠的质量为x,生成氢气、氢氧化钠的质量分别为y、z。
2NaCl + 2H2O Cl2
↑+ H2 ↑+ 2NaOH
117
71 2 80
x
7.1g y z
…………………………………… 1分
117:x = 71:7.1g x=11.7g
2:y = 71:7.1g y=0.2g
…………………………………… 1分
80:z
= 71:7.1g z=8g
…………………………………… 1分
剩余氯化钠的质量=100g×25%-11.7g=13.3g …………………………………… 1分
⑵反应后溶液的质量=100g-7.1 g -0.2g=92.7g …………………… 1分
 …………………………………… 1分
…………………………………… 1分
答:⑴生产氢气的质量是0.2g,剩余氯化钠的质量是13.3g。
⑵反应后所得溶液中氢氧化钠的质量分数是8.63%。
注:方程式不配平或缺少必要的反应条件均不给分;20、21题化学符号书写不规范另扣1分。

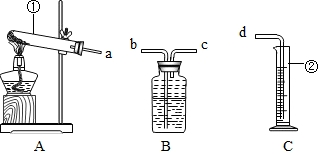
 某校化学兴趣小组的同学利用下图所示装置进行实验.
某校化学兴趣小组的同学利用下图所示装置进行实验.