
题目列表(包括答案和解析)
| 加热 |
| 加热 |
| 点燃 |
| 点燃 |
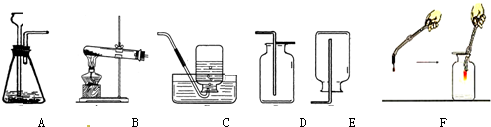
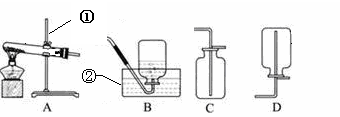 实验室用高锰酸钾制取氧气,根据下列装置回答问题:
实验室用高锰酸钾制取氧气,根据下列装置回答问题:
(1)写出图中有编号的仪器名称:
① ,②
(2)某同学用高锰酸钾制取并收集氧气,他选择上述装置中的A和装置B进行组装。
你认为A装置中还缺少_____ _。其作用: 。
写出该反应的文字表达式:______ _______ ;该反应类型是: 。
(3)在装药品之前必须进行的操作是: 
(4)连接装置A和装置B制取氧气时,开始收集氧气的最适宜时刻是: 。
判断氧气已收集满的现象是:
(5)用排水法收集氧气完毕,停止实验时,应先 ,后 ,其目的是防止 。
(6)某同学制取并用排水法 收集了一瓶气体,然后往集气瓶中伸入带火星的木条,只看到火星亮了一些,导致这种现象的原因可能是(任写一种)
收集了一瓶气体,然后往集气瓶中伸入带火星的木条,只看到火星亮了一些,导致这种现象的原因可能是(任写一种)
实验目的:(1)用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验。
(2)粗略测定加热2 g高锰酸钾所收集到的氧气体积。
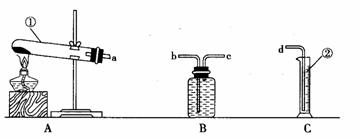
(1)写出加热高锰酸钾制氧气的化学方程式:
细铁丝在氧气中燃烧化学方程式:__________ ______。
(2)装置连接:为达到实验目的(2),各装置的正确连接顺序是:(填接口的字母)
a→( )( ) →d
(3)实验过程发现B瓶中的水变红了,原因是:____________ ___
(4)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作可能是:
____________________________________________________________
(5)铁丝在氧气中燃烧实验中
①铁丝为什么要绕成螺旋状? 。
②铁丝前端为什么要系一根火柴? 。
③点燃火柴后,铁丝插入集气瓶中的适宜时刻是 。
(6)为何铁丝要由上而下缓慢伸入集气瓶中 。
(7)在研究“适于制取氧气的物质及其反应条件”的过程中,某同学完成了下表所示系列实验:
| 序号 | 实验 | 能否生成氧气 |
| A | 加热高锰酸钾 | 能 |
| B | 加热二氧化硅 | 不能 |
| C | 加热氯化钠 | 不能 |
| D | 加热水 | 不能 |
| E | 电解水 | 能 |
①根据实验A、B、C,可以得出的结论是:在一定条件下, ;
② 根据实验D、E,可以得出的结论是: 是影响物质能否反应产生氧气的重要因素;
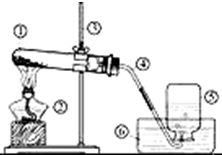 如图是高锰酸钾制取氧气的装置图.
如图是高锰酸钾制取氧气的装置图.实验室用高锰酸钾制氧气,并用排水法收集,试回答下列问题:
(1)制取氧气前要检查装置的气密性,目的是防止装置________.
(2)伸入盛高锰酸钾的试管里的导管不宜过长,原因是________.
(3)在试管口处放一团棉花,其目的是________.
(4)加热时先将酒精灯在试管下方来回移动,其目的是________.
(5)用排水法收集时,当________时再开始收集.
(6)集满氧气的集气瓶应在________盖好玻璃片,取出________(填“正”或“倒”)放在桌面上.
(7)实验完毕,应先________,再________,其目的是________.
第Ⅰ卷 选择题(共38分)
一、(本题包括14小题,每小题2分,共28分。每小题只有一个选项符合题意。)
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
答案
D
D
B
A
A
B
D
B
A
B
B
D
A
B
二、(本题包括5小题,每小题2分,共10分。每小题只有一个或两个选项符合题意。若正确答案包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的给1分,选两个且都正确的给2分,但只要选错一个,该小题就为0分。)
题号
15
16
17
18
19
答案
BC
B
A
AB
A
第Ⅱ卷 非选择题(共62分)
三、(本题包括10小题,共56分,每空1分)
|