
̀âÄ¿Áбí(°üÀ¨´đ°¸ºÍ½âÎö)
| A¡¢1£º1£º1 | B¡¢3£º2£º1 | C¡¢1£º2£º3 | D¡¢2£º3£º6 |

| c2(C) |
| c(A)¡Ác(B) |
| c2(C) |
| c(A)¡Ác(B) |
| ÈƯÆ÷ | ¼× | ̉̉ | ±û |
| ÆđʼͶÁÏ | 1molAºÍ1molB | 2molC | 2molAºÍ2molB |
| AµÄƽºâŨ¶È | C1 | C2 | C3 |

| ÈƯÆ÷ | ¼× | ̉̉ | ±û |
| ÆđʼͶÁÏ | 1molAºÍ1molB | 2molC | 2molAºÍ2molB |
| AµÄƽºâŨ¶È | C1 | C2 | C3 |
ij»¯Ñ§ĐËÈ¤Đ¡×éÉè¼ÆÓĂʵÑéỂÀïµÄ³£¹æ̉ÇÆ÷ÖÆÈ¡ÉÙÁ¿Æ¯°×·Û¡£¿É̉ÔÑ¡ÓõÄ̉ÇÆ÷ÓĐA¡«H£¬ÆäÖĐ·Ö̉ºÂ©¶·Àï¾ùÊ¢ÓĐŨÑÎËᣬAµÄ´óÊÔ¹ÜÀï¼°ÉƠÆ¿ÖĐ¾ù×°ÓĐ̉»¶¨Á¿µÄ¶₫Ñơ»¯Ằ¹̀̀壬BºÍHµÄUĐιÜÄÚ¾ù×°ÓĐÏûʯ»̉£¬BµÄË®²ÛÀïÊ¢ÓбùË®£¬DÖĐ×°ÓĐ³ÎÇåʯ»̉Ë®£¬EÖĐ×°ÓĐŨÇâÑơ»¯ÄÆÈÜ̉º¡£̉ÑÖª£¬ÂÈÆøÓëÇâÑơ»¯¸ÆµÄ·´Ó¦ÊÇ·ÅÈȵģ¬¶øÔÚζÈÉÔ¸ßʱÂÈÆøÓëÇâÑơ»¯¸Æ¾Í»á·¢Éú¸±·´Ó¦¶øÉú³ÉÂÈËá¸ÆµÈ¸±²úÎï¡£
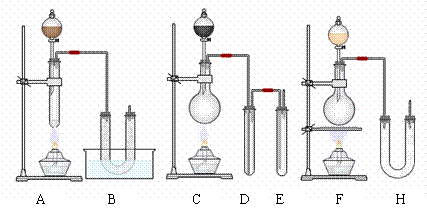
£¨1£©ÇëÄă¸ù¾Ưʵ¼ÊĐè̉ª£¬´ÓA¡«HÖĐÑ¡³ö×îºÏÀíµÄ̉ÇÆ÷×é×°³É̉»̀×ÖÆÈ¡ÉÙÁ¿Æ¯°×·ÛµÄʵÑé×°ÖĂ£¨ÓĂĐ̣ºÅ±íʾ£¬²¢̉ª°´ƠƠ×îºÏÀíµÄ˳Đ̣´Ó×óµ½Ó̉ÅÅÁĐ£© ¡£
£¨2£©ÈôÓÉAB×é³ÉµÄ×°ÖĂÊǼ×ͬѧÉè¼ÆµÄ£¬ÓÉCDE×éºÏ³ÉµÄ×°ÖĂÊÇ̉̉ͬѧÉè¼ÆµÄ£¬ÓÉFH×éºÏ³ÉµÄ×°ÖĂÊDZûͬѧÉè¼ÆµÄ£¬ÇëÄă·ÖÎö¼×¡¢̉̉¡¢±ûÈừ××°ÖõÄÓÅȱµă¡£
| ×°ÖĂĐ̣ºÅ | Óŵă | ȱµă |
| ¼× | ||
| ̉̉ | ||
| ±û |
1.B 2.D 3.C 4.C 5.D 6.B 7.AD 8.BC 9.CD 10.D 11.A 12.C 13.BC 14.C
15.C 16.B 17.B 18.D
19£®£¨1£©¢Ú¢Û¢Ư £¨2£©¢Ù¢Ú¢Û¢Ü¢̃ £¨3£©¢Ù¢Ú¢ß £¨4£©ÔÚAÖĐ¼ÓÂúË®£¬¸Ç½ôÆ¿Èû£¬ÓĂ½º¹ÜÁ¬½ÓbºÍc½Ó¿Ú£¬ÊƠaµ¼ÈëNOÆø̀壬ˮͨ¹ưbºÍcµ¼ÈëBÖĐ¡£
20£®£¨1£©¼×ͬѧµÄ½áÂÛ²»ƠưÈ·¡£SO2ÓĐ»¹ÔĐÔ£¬²úÎïÓĐ¿ÉÄÜÊÇNa2SO4£¬Í¬Ê±SO2ÖĐÓĐË®ƠôÆø£¬̉²»áÓëNa2O2·´Ó¦²úÉúO2¡££¨2£©¢Ù³ưË®ƠôÆø¸ÉÔïSO2£»ÎüÊƠδ·´Ó¦µÄSO2¡£¢Ú²»ºÏÀí¡£Ï¡HNO3Äܽ«BaSO3Ñơ»¯ÎªBaSO4£»Èç¹û·´Ó¦ºóµÄ¹̀̀åÖĐ»¹²ĐÁôNa2O2£¬ËüÈÜÓÚË®ºóÄܽ«ÑÇẠ́Ëá¸ùÑơ»¯³ÉẠ́Ëá¸ù¡£
21£®£¨1£©S¡¢H2S¡¢SO2¡¢SO3¡¢H2SO4 £¨2£©N2¡¢NH3¡¢NO¡¢NO2¡¢HNO3
£¨3£©3Cu+8H++2NO3¨D 3Cu2++2NO¡ü+4H2O
22£®£¨1£©(NH4)2SO3(»̣NH4HSO3); (NH4)2SO4(»̣NH4HSO4); SO2; NH3; K2SO3; K2SO4
£¨2£©SO32¨D+Br2+H2O SO42¨D+2Br¨D+2H+
23£®£¨1£©½đ¸Ơʯ¡¢Ê¯Ó¢¡¢²£Á§ £¨2£©SiO2+2NaOH Na2SiO2+H2O
Na2CO3+SiO2 Na2SiO3+CO2¡ü CaCO3+SiO2 CaSiO3+CO2¡ü
24£®£¨1£©¹²¼Û¼ü NH3 Èư½Ç׶ĐÎ £¨2£©3NO2+H2O=2HNO3+NO
£¨3£©N2£¨g£©+H2£¨g£© NH3£¨g£©£»¡÷H=£46.2kJ?mol¨D1 £¨4£©8NH3+Cl2=N2+6NH4Cl
25£®£¨1£©N2O£¬NO2£¬NO£»1: 3: 5 £¨2£©1.08mol
26£®£¨1£©¢Ù>2£»4b£»a£2b£»H2S£¨Na2S¹ưÁ¿£© ¢Ú=2£»2a£¨»̣4b£©£»O£»Î̃£¨ƠưºĂ·´Ó¦£©
¢Û<2£»£»SO2£¨Na2S2O3¹ưÁ¿£© £¨2£©a=3b
¹ú¼ÊÑ§Đ£ÓÅÑ¡ - Á·Ï°²áÁбí - ÊỒâÁбí
º₫±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨Æ½̀¨ | ÍøÉÏÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | µçĐÅƠ©Æ¾Ù±¨×¨Çø | ÉæÀúÊ·ĐéÎ̃Ö÷̉åÓĐº¦ĐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ĐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com