
题目列表(包括答案和解析)
| O | - 4 |
| O | 2- 4 |

 图所示装置的减压过滤与母液分离.
图所示装置的减压过滤与母液分离.| O | 2- 4 |
对于某些离子的检验及结论一定正确的是( )
A.向待检液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定含有SO42-
B.向待检液中加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有NH4+
C.向待检液中加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定含有大量的CO32-
D.向待检液中加入加入几滴氯水,再加入KSCN溶液,溶液立即变红,则原溶液中一定含有Fe3+
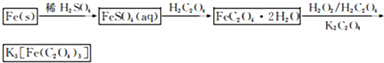
K3[Fe(C2O4)3]·3H2O [三草酸合铁(Ⅲ)酸钾晶体]易溶于水,难溶于乙醇,可作为有机反应的催化剂。实验室可用铁屑为原料制备,相关反应过程如下,请回下列问题:

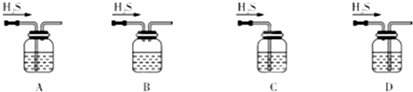
(1)铁屑中常含硫元素,因而在制备FeSO4时会产生有毒的H2S气体,该气体可用氢氧化钠溶液吸收。下列吸收装置正确的是 。

(2)在得到的FeSO4溶液中需加入少量的H2SO4酸化,目的是 ,得到K3[Fe(C2O4)3]溶液后,加入乙醇的目的是 。
(3)晶体中所含结晶水可通过重量分析法测定,主要步骤有:①称量,②置于烘箱中脱结晶水,③冷却,④称量,⑤重复②~④至恒重,⑥计算。
步骤③需要在干燥器中进行的原因是 ;
步骤⑤的目的是 。
(4) 可被酸性KMnO4溶液氧化放出CO2气体,所以实验产物中K3[Fe(C2O4)3]·3H2O含量测定可用KMnO4标准溶液滴定。
可被酸性KMnO4溶液氧化放出CO2气体,所以实验产物中K3[Fe(C2O4)3]·3H2O含量测定可用KMnO4标准溶液滴定。
①写出滴定过程中发生反应的离子方程式 ;
②下列滴定操作中使滴定结果偏高的是 ;
A.滴定管用蒸馏水洗涤后,立即装入标准液
B.锥形瓶在装待测液前未用待测液润洗
C.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
D.读取标准液体积时,滴定前仰视读数,滴定后俯视读数
③取产物10.0g配成100mL溶液,从中取出20mL于锥形瓶中,用浓度为0.1mol·L-1酸性KMnO4溶液滴定,达到滴定终点时酸性KMnO4溶液消耗24mL,计算产物中K3[Fe(C2O4)3]·3H2O的质量分数 。[已知摩尔质量M(K3[Fe(C2O4)3]·3H2O)=491g·mol-1]
对于某些离子的检验及结论一定正确的是( )
A.向待检液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定含有SO42-
B.向待检液中加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体生成,则原溶液中一定含有NH4+
C.向待检液中加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定含有大量的CO32-
D.向待检液中加入加入几滴氯水,再加入KSCN溶液,溶液立即变红,则原溶液中一定含有Fe3+
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com