
题目列表(包括答案和解析)
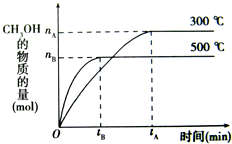 一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g)?CH3OH(g)达到平衡状态.
一定条件下,在体积为3L的密闭容器中化学反应CO(g)+2H2(g)?CH3OH(g)达到平衡状态.| c(CH3OH) |
| c(CO)×c2(H2) |
| c(CH3OH) |
| c(CO)×c2(H2) |
| ||
| tB |
| ||
| tB |
| 1 |
| 2 |
 ,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).
,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).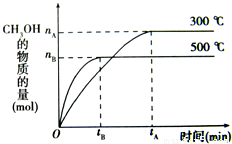
 ,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).
,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).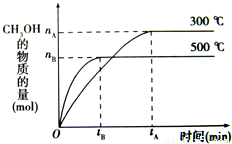
 ,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).
,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).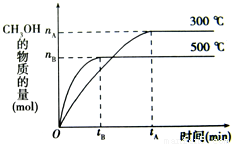
 ,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).
,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母).
必考卷
第Ⅰ卷
一、选择题:每小题3分,共45分
题号
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
答案
A
C
D
C
C
D
B
A
B
B
A
A
D
D
C
第Ⅱ卷
二、填空题:
16.(10分)
每空2分,化学方程式、离子方程式没有配平不给分,条件未标扣1分,沉淀、气体符
号未标不扣分。
(1)O
(2)
(3)


(4)
(5)O=C=O
17.(10分)
每空2分,化学方程式、离子方程式没有配平不给分,条件未标扣1分,沉淀、气体符
号未标不扣分。
(1) 
(2)第三周期第ⅥA族
(3)氧,B
(4)
18.(12分)
实验一
(1)胶头滴管、250mL容量瓶 (每空1分,共2分)
(2)0.2000mol?L (2分)
(2分)
实验二
(1)0.0100mo1?L 醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于l
醋酸的pH大于2或醋酸稀释10倍时,pH的变化值小于l
(3分,其它合理答案酌情给分)
(2)增大 、(2分)
实验三
答:用pH计(或pH试纸)测定相同浓度的醋酸在几种不同'温度时的pH(3分其他合
19.(10分)
每空2分,其它合理答案酌情给分
(1)
(2)CD
(3)
(4)甲醇、氢氧化钠、水(答出甲醇即给2分) 
选考卷
20(A).(13分)
(1)分子晶体 (2分)
(2)没有 (2分)
(3) . (3分)
. (3分)
(4)O N C (2分)
(5) 键和
键和 键 (2分)
键 (2分)
(6)CO中断裂第一个 键消耗的能量(273
kJ?mol
键消耗的能量(273
kJ?mol )比N
)比N 中断裂第一个
中断裂第一个 键消耗的能量(523.3kJ?mol
键消耗的能量(523.3kJ?mol )小,CO的第一个键较容易断裂,因此CO较活泼。(其它合理答案酌情给分)(2分)
)小,CO的第一个键较容易断裂,因此CO较活泼。(其它合理答案酌情给分)(2分)
20(B).(13分)
(1)羟基,羧基(2分)
(2)消去反应(2分)
(3) 
(4) 
(5) 4 (2分)
(6) 
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com