
题目列表(包括答案和解析)
1(11分) 按要求填空:
(1) 含有18种元素的周期是第____________周期。
(2) 周期表中最活泼的金属元素位于第_____________纵行。
(3) 写出分子具有双核18电子的物质与水反应的化学方程式
_______________________________________________________________________。
(4) 周期表前20号元素中,某两种元素的原子序数相差3,周期数相差1,它们形成化合物时原子数之比为1∶2。写出这些化合物的化学式:(至少写4种)_______________。
 M、N、X、Y四种主族元素在周期表里的相对位置如图所示,已知它们的原子序数总和为46.
M、N、X、Y四种主族元素在周期表里的相对位置如图所示,已知它们的原子序数总和为46.

| ||
| ||
| 质子数 | 16 | 16 | 16 |
| 电子数 | 16 | 17 | 18 |
| 化学式 |
A、B、C、D、E、F六种短周期主族元素,其核电荷数依次增大,已知元素A和C可形成两种常温下均为液体的化合物,B原子最外层电子数是最内层电子数的两倍,A与D、C与F分别处于同一主族且A、D质子数之和是C、F质子数之和的一半,18gE与足量盐酸反应生成标准状况下的H222.4L。
请按要求回答:
(1)由A、C、D三种元素形成的化合物X中含有的化学键类型为_______。
(2)A、D、F三种元素形成的化合物Y溶液中的微粒浓度之间存在如下关系(请填写下式中的空白,每空只填一种微粒浓度的符号)。
c(H+)+_______:c(OH―)+ _______。
(3)E、F构成的化合物能与水反应,写出化学方程式_______。
(4)①写出单质D与乙醇反应的化学方程式_______。
②A、B、C三种元素可以形成最简式为A4B2C的有机物,该有机物与足量X水溶液反应得到的两种产物中含有相同数目的B原子。写出该反应的化学方程式_____。
(5)A和B组成的化合物M,每个分子中含有18个电子,常温常压下,0.5molM完全燃烧放出780kJ的热量,请写出表示M完全燃烧的热化学方程式____。
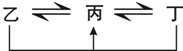 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.图中均含D或F元素的物质均会有图示转化关系:(12分)有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属。A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、空间构型为三角锥形,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族。下图中均含D或F元素的物质均会有图示转化关系:
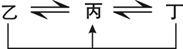
①均含D元素的乙、丙、丁微粒间的转化全为非氧化还原反应;
②均含F元素的乙(单质)、丙、丁微粒间的转化全为氧化还原反应。请回答下列问题:
(1)化合物甲的电子式为 。
(2)F元素在周期表中的位置 ;稳定性:A2C A2E(填“大于”“小于” “等于”)。
(3)均含有D元素的乙与丁在溶液中发生反应的离子方程式 。
(4)丙、丁分别是含F元素的简单阳离子,检验含丙、丁两种离子的混合溶液中的低价离子,可以用酸性KMnO4溶液,其对应的离子方程式为:
(5)已知常温下化合物FE的Ksp=6×10-18 mol2·L-2,常温下将1.0×10-5mol·L-1的Na2E溶液与含FSO4溶液按体积比3 :2混合,若有沉淀F E生成,则所需的FSO4的浓度要求 。(忽略混合后溶液的体积变化)。
一、单项选择题(本题包括12小题,每小题4分,共48分。每小题只有一个选项符合题意)
题号
1
2
3
4
5
6
7
8
9
10
答案
D
B
D
A
B
A
C
B
D
C

 22.(14分)
(1) O、H、S、Cl 硫酸(4分)
22.(14分)
(1) O、H、S、Cl 硫酸(4分)
(2) (3分)
(3) SO2 + 2H2O + Cl2 = 4H++ SO42-+ 2Cl-(3分)
SO2和Cl2按相等物质的量通入品红溶液(2分)
(4) Fe + S
 FeS,2Fe + 3Cl2
FeS,2Fe + 3Cl2
 2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
2FeCl3(或Cl2 +
H2S = S↓+ 2HCl
或Cl2 + Na2S S↓+ 2NaCl)(2分)
四、实验题(本大题共2小题,共21分)
23.(5分)
(1)同周期
(2)同主族
Ⅰ
A、F、H
E、D
Ⅱ
d、c、b
g、f
24.(16分) (1) 分液漏斗上口的塞子未打开(或漏斗未与大气相通或漏斗塞子的凹槽未与颈部的通气孔对准。(2分)
(2) ④ (2分)
(3) 溶液由红色褪为无色,SO2 + OH- = HSO3-或SO2 + 2OH-= SO32-+ H2O。 (4分)
(4) 产生白色沉淀,SO2被HNO3氧化产生SO42-,与Ba2+产生白色沉淀。(4分)
(5) ① 关闭K2,在烧杯中用水封住玻璃导管口,用手捂住集气瓶b,烧杯中导管口有气泡产生,松手后,导管内有一段液柱保持不降则气密性好。(2分)
② 打开K1,关闭K2,点燃酒精灯。(2分)
五、计算题(本大题共1个小题,共11分)
25.(1) S H2S Na2S2O3 + H2SO4 = Na2SO4 + SO2 + S↓+ H2O
Na2S + H2SO4 = Na2SO4 + H2S↑ 2H2S+SO2=3S↓+2H2O(各1分)
(2) Na2S2O3 :0.025 mol Na2S:0.075 mol(各3分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com