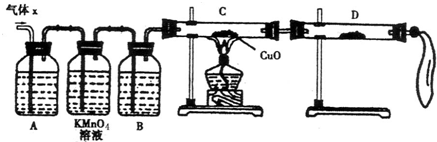
不同的金属在化学反应中表现出来的活泼程度不同,早在1812年瑞典化学家贝采里乌斯根据大量实验现象首先提出了金属活动顺序的概念,后来俄国化学家贝开托夫在大量实验和系统研究之后,于1865年发表了金属活动性顺序:K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au.
(1)金属活动性顺序是学习“金属及其化合物”的重要工具,许多“金属及其化合物”的知识规律可以通过金属活动性顺序来掌握.例如,工业上冶炼金属,根据金属活动性顺序可以采用不同的冶炼方法.其中可以用“热分解法”冶炼的金属是
Hg
Hg
、
Ag
Ag
.
工业上又常用下列反应进行金属钾的冶炼:Na+KCl
K↑+NaCl,似乎“违背”了金属活动性顺序,试解释钠能将更活泼的钾置换出来的原因
该反应为可逆反应,及时抽出钾蒸气,导致平衡不断正向移动
该反应为可逆反应,及时抽出钾蒸气,导致平衡不断正向移动
.
(2)在实践中发现还有许多化学事实“违背”金属活动性顺序,但这些“反常”现象都可以通过化学原理得到合理解释.某学生在做探究实验时,把锌粒投入1mol?L
-1氯化铁溶液中,观察到如下实验现象:锌粒表面有一定量气泡产生,溶液颜色逐渐变浅,一段时间后溶液逐渐浑浊,试用相关反应方程式进行解释
Zn+2Fe3+═Zn2++2Fe2+
Zn+2Fe3+═Zn2++2Fe2+
、
3Zn+2Fe3++6H2O═2Fe(OH)3↓+3H2↑+3Zn2+[或Fe3++3H2O?Fe(OH)3+3H+,Zn+2H+═Zn2++H2↑,或写化学方程式也可以]
3Zn+2Fe3++6H2O═2Fe(OH)3↓+3H2↑+3Zn2+[或Fe3++3H2O?Fe(OH)3+3H+,Zn+2H+═Zn2++H2↑,或写化学方程式也可以]
.
(3)研究金属活动性顺序还可以指导对金属阳离子氧化性强弱的认识,工业上用氯化铁溶液腐蚀铜制电路板.
①请根据金属活动性顺序结合该反应原理,比较Cu
2+、Fe
3+、Fe
2+的氧化性强弱
Fe3+>Cu2+>Fe2+
Fe3+>Cu2+>Fe2+
.
②请运用原电池原理设计实验验证Cu
2+、Fe
3+氧化性强弱的结论.
方案:
铜棒与碳棒用导线连接,再插入氯化铁溶液,发现有电流产生,铜棒不断溶解,溶液由黄色变为蓝色或蓝绿色
铜棒与碳棒用导线连接,再插入氯化铁溶液,发现有电流产生,铜棒不断溶解,溶液由黄色变为蓝色或蓝绿色
.