
题目列表(包括答案和解析)
标准状况下,a L Cl2通入到1 L b mol/L的FeI2溶液中,充分反应后,所得溶液中Fe2+的物质的量浓度与a、b的关系如下表,请完成其余空格。
a、b的关系 | Fe2+的物质的量浓度(mol/L) |
a≤22.4b | ① b |
②a≥33.6b | 0 |
22.4b≤a≤33.6b | ③ |
【解析】根据微粒的还原性的相对强弱顺序:I->Fe2+>Br-,所以Cl2通入溶液中,①首先是将I-氧化成I2,②剩余的Cl2才可能将Fe2+氧化成Fe3+,即:
①FeI2+Cl2 FeCl2+I2
FeCl2+I2
②2FeCl2+Cl2 2FeCl3
2FeCl3
总反应为:2FeI2+3Cl2 2FeCl3+2I2
2FeCl3+2I2
从以上反应方程式不难看出:
当n(Cl2)≤n(FeI2)时,只有I-被氧化,Fe2+的浓度保持不变;
当n(Cl2)>n(FeI2)时,I-全被氧化,Fe2+部分或全部被氧化。
故Fe2+的浓度有如下三种情况:
(1)![]() ≤b mol,a≤22.4b c(Fe2+)=b mol/L
≤b mol,a≤22.4b c(Fe2+)=b mol/L
(2)![]() :b mol≥3∶2,a≥33.6b时,Fe2+全部被氧化,c(Fe2+)=0
:b mol≥3∶2,a≥33.6b时,Fe2+全部被氧化,c(Fe2+)=0
(3)22.4b≤a≤33.6b,Fe2+部分氧化c(Fe2+)=b-(![]() -b)×2 mol/L
-b)×2 mol/L
能源、可划分为一级能源和二级能源。自然界中以现成形式提供的能源,击。煤、石油、天然气称为一级能源需依靠其他能源的能量间接制取的能源称为二级能源。煤、石油、天然气等是多年来大规模使用的能源,称为常规能源,属于不可再生的化石能源。一些著名的地质专家预测,石油产量最早可能在2010年,最迟在2037年达到顶峰。此后就会不可逆转地下降,而石油和天然气的价格将大幅上升,且难以回落。
煤、石油、天然气等化石燃料燃烧后会放出多种污染大气的化学物质以及二氧化碳等温室气体,而氢燃料电池源源不断地提供能量的同时排出的只有水。
美国加州理工学院的研究员在美国《科学》上撰文指出,氢燃料系统未必对环境完全无害。氢比空气轻得多,很容易向空中运动。研究员们估计完全使用氢燃料将导致进入大气同温层的氢分子增加到目前的3倍。同温层距地面15-40km,包含臭氧层,氢分子进入同温层会被氧化成水。
发展氢燃料系统的主要提倡者杰里米?里夫金说:“当转而利用一种新能源的时候,你必然设想它可能产生一些环境影响,但是氢作为化石燃料的替代物,依然是我们未来的希望。”
发展氢能源需要解决如何廉价地制备大量氢气,以及如何安全贮存、运输氢气等问题。从化石原料制取氢气,已经有比较成熟的技术及工业装置,并在不断研究改进之中,所制得的氢气主要作为化工原料,如合成氨、合成甲醇及油品等。但从化石原料制取氢气的过程必然会放出二氧化碳,因此不能解决温室气体的排放问题。非化工原料制氢主要是指从含氢物质制取氢气,其中水电解制氢技术已成熟并有工业生产装置,但电能消耗较大(每立方米氢气耗电约4~5kw-h),目前尚受到一定的限制。但从水中制氢是理想的制氢方法。
【思考】阅读以上文摘,并注意带有下划线的文字,完成下列填空。
(1)理想的制氢方法是 ,此过程是 (填写“释放”或“消耗‘)能量的过程。氢气是一种高效而又没有污染的 级能源。
(2)水电解制氢反应的化学方程式是 。
(3)关于用水制取氢气,以下研究方向不正确的是
A.构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找特殊化学物质,用于开发廉价能源,以分解水获得氢能源
(4)作为能源,氢气具有其他能源所不具备的优点。第一,燃烧时放出的热量多,放出的热量约为同质量汽油的3倍。第二 。第三最大的优点是 。氢气的重量轻、密度小,便于运送和携带,容易储藏,与难储存的电相比,优越性更为显著。
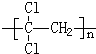 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由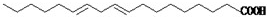 ]对人体健康是十分有益的,然而,市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
]对人体健康是十分有益的,然而,市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
| 双原子分子 | 三原子分子 | 四原子分子 | 五原子分子 | ||||
分子 | H2 | HCl | H2O | CO2 | BF3 | NH3 | CH4 | CH3Cl |
键的极性 |
|
|
|
|
|
|
|
|
键角 | - | - |
|
|
|
|
| - |
空间构型 |
|
|
|
|
|
|
|
|
分子极性 |
|
|
|
|
|
|
|
|
根据以上分析结果,试推测以上哪些物质易溶于水__________________________________。
| 分子 | 键的极性 | 键角 | 空间构型 | 分子极性 |
单原子分子 | He、Ne | — | — | — |
|
双原子分子 | H2 |
| — |
|
|
HCl |
| — |
|
| |
三原子分子 | H2O |
|
|
|
|
CO2 |
|
|
|
| |
四原子分子 | BF3 |
|
|
|
|
NH3 |
|
|
|
| |
五原子分子 | CH4 |
|
|
|
|
CH3Cl |
|
|
|
|
根据以上分析结果,试推测以上哪些物质易溶于水____________________ 。?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com