
题目列表(包括答案和解析)
 )在镍催化剂作用下加1 mol氢气,转变成乳酸,乳酸的结构简式是____________。
)在镍催化剂作用下加1 mol氢气,转变成乳酸,乳酸的结构简式是____________。(2)与乳酸具有相同官能团的乳酸的同分异构体A在酸性条件下,加热失水生成B,由A生成B的化学反应方程式是____________________________________。
(3)B的甲酯可以聚合,聚合物的结构简式是________________________。
1,3―丙二醇是重要的化工原料,用乙烯合成1,3―丙二醇的路线如下:
CH2=CH2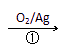
![]()
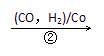 HOCH2CH2CHO
HOCH2CH2CHO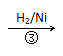 HOCH2CH2CH2OH
HOCH2CH2CH2OH
⑴通过反应①用乙烯和空气混合气体制备![]() ,测得反应前和某一时刻气体的体积分数如下表。
,测得反应前和某一时刻气体的体积分数如下表。
| C2H4 | O2 | N2 |
| |
| 反应前体积分数 | 25.0% | 15.0% | 60.0% | 0 |
| 某一时刻体积分数 | 5.56% | 5.54% | 66.7% | 22.2% |
计算此时乙烯的转化率。
⑵某化工厂已购得乙烯14t,考虑到原料的充分利用,反应②、③所需的CO和H2可由以下两个反应获得:
C+H2O![]() CO+H2 CH4+H2O
CO+H2 CH4+H2O![]() CO+3H2
CO+3H2
假设在生产过程中,反应②中CO和H2、反应③中H2均过量20%,且反应①、②、③中各有机物的转化率均为100%。
计算至少需要焦炭、甲烷各多少吨,才能满足生产需要?
(15分)
1-1 2011年是国际化学年,是居里夫人获得诺贝尔化学奖100周年。居里夫人发现的两种化学元素的元素符号和中文名称分别是 和 。
1-2 向TiOSO4水溶液中加入锌粒,反应后溶液变为紫色。在清夜中滴加适量的CuCl2水溶液,产生白色沉淀。生成白色沉淀的离子方程式是 ;继续滴加CuCl2水溶液,白色沉淀消失,其离子方程式是 。
1-3 20世纪60年代维也纳大学V.Gutmann研究小组报道,三原子分子A可由SF4和NH3反应合成;A被AgF2氧化得到沸点为为27℃的三元化合物B。A和B分子中的中心原子与同种端位原子的核间距几乎相等;B分子有一根三种轴和3个镜面。画出A和B的结构式(明确示出单键和重键,不在纸面上的键用楔形键表示,非键合电子不必标出)。
1-4 画出Al2(n-C4H9)4H2和Mg[Al(CH3)4]2的结构简式。
1-5 已知EӨ(FeO42—/Fe3+) = 2.20V,EӨ(FeO42—/Fe(OH)3) =0.72 V。
① 写出氯气和三氯化铁反应形成高铁酸根的离子方程式。 。
② 写出高铁酸钾在酸性水溶液中分解的离子方程式。 。
③ 用高铁酸钾与镁等组成碱性电池,写出该电池的电极反应 。
(18分)
|

 ;
;(18分)(1)1 mol O2与足量氢气反应产生水蒸气放热483.6 kJ,若1 g水蒸气转化成液态水放热2.444 kJ,请写出表示氢气燃烧热的热化学方程式:__________________________________。
(2)由汽油裂解得到乙烯、丙烯是重要的化工原料,请写出下列转化的方程式,并注明反应类型。
丙烯 → 聚丙烯
___________________________________________________
(3)将N2、H2置于容积为2L的密闭容器中,发生反应,反应进行到4S末,测得N2 2mol 、H21.5mol、NH32mol。则用氮气浓度的减少来表示该反应速率为__________ 。
(4)在500ml密闭容器中,将2mol A和1molB混合加热到500℃,达到平衡
2 A(g) +B (g) 3C(g) K = 16求A转化为C的转化率为__________。
3C(g) K = 16求A转化为C的转化率为__________。
(5) 在密闭容器中发生下列反应:aA(g)  cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a _______ c+d(填“>”、“=”或“<”)。
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,A的浓度为原平衡的2.1倍,则 a _______ c+d(填“>”、“=”或“<”)。
(6) 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如下图,反应的化学方程式为______________________________________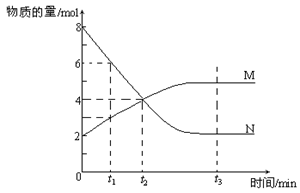
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com