
题目列表(包括答案和解析)
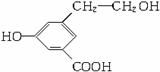
(1)有机物A在稀H2SO4作用下水解只生成一种产物B,试写出B的结构简式___________,B分子中所含官能团的名称是___________、___________。
(2)B不可能发生的反应是___________(填序号)。
①加成 ②酯化 ③加聚 ④氧化 ⑤消去 ⑥取代
(3)写出B与浓溴水反应的化学方程式:________________________________________。
(4)等物质的量的B分别与足量的Na、NaOH溶液、NaHCO3溶液充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为___________。
(5)B和C互为同分异构体,C物质苯环上的一氯代物只有两种,C不与NaHCO3反应,能与Na、NaOH溶液反应,等物质的量的C消耗Na、NaOH的物质的量之比为2∶3,则C可能有的结构简式为:___________________________________________________________。
(7分)物质A的结构简式为
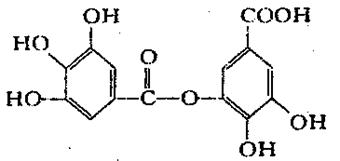
(1)A的分子式为
![]() (2)有机物B在硫酸催化条件下加热发生酯化反应可得到A。则B的结构简式为 。
(2)有机物B在硫酸催化条件下加热发生酯化反应可得到A。则B的结构简式为 。
![]() (3)请写出A与过量NaOH溶液反应的化学方程式 。
(3)请写出A与过量NaOH溶液反应的化学方程式 。
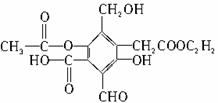
(1)A与过量NaOH完全反应时,A与参加反应的NaOH物质的量之比为____________。
(2)A与新制Cu(OH)2完全反应时,A与参加反应的Cu(OH)2物质的量之比为_________,其中A与被还原的Cu(OH)2的物质的量之比为__________。
(3)A与过量NaHCO3完全反应时,A与参加反应的NaHCO3物质的量之比为___________。

从A出发,可以发生下列所示的一系列反应,其中K的分子式为C12H14O4,L和K互为同分异构体,F的产量可作为衡量一个国家石油发展水平的标志。
请完成下列问题:
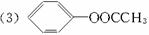
(1)FH的反应类型是_________。
(2)下列物质的结构简式:
B:_________;K:_________;L:_________。
(3)写出与B互为同分异构体,且苯环上只有一个取代基的各有机物的结构简式。

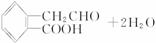
请回答下列问题:
(1)A→C的反应类型为_________________,A→D的反应条件是_________________。
(2)在A—E五种物质中,互为同分异构体的是_________________(填代号)。
(3)写出由A生成B的化学方程式__________________________________。
(4)已知HCHO分子中所有原子都在同一平面内,则在上述分子中所有的原子有可能都在同一平面的物质是_____________(填序号)。
(5)C能形成高聚物,该高聚物的结构简式为_________________。
(6)写出D与NaOH溶液共热反应的化学方程式__________________________________。
一、选择题(本题包括9小题,每小题3分,共27分。每小题只有一个选项符合题意。)
题号
1
2
3
4
5
6
7
8
9
答案
D
A
B
C
D
B
C
B
D
二、选择题(本题包括9小题,每小题4分,共36分。每小题有一个或两个选项符合题意。若正确答案包括两个选项,只选一个且正确的给2分,但只要选错一个,该小题就为0分。)
题号
10
11
12
13
14
15
16
17
18
答案
AC
AD
AB
C
D
C
AD
B
C
三.(本题包括3小题,,共34分)
19.(14分)
(1)烧杯、玻璃棒,过滤,换过滤器并重新进行过滤操作(4分,每空1分)
(2)NaOH、Na2CO3(2分) (其他合理的试剂也可给分)
(3)NaOH , C (2分,各1分)
(4)除去NaOH和Na2CO3(2分)
(5)蒸发皿,蒸发皿中有大量固体析出(2分,各1分)
(6)加快沉淀生成 , 5.61×10―8 mol?L―1。(2分,各1分) ]
20.(7分)
(1)掩蔽Fe3+,防止造成偏大的误差(1分)
(2)提供酸性条件,抑制Cu2+的水解(1分)
(3)防止空气中的氧气与碘化钾反应(1分)
(4)2Cu2++4I-=2CuI↓+I2 (2分)
(5)ω(Cu)= 64CV/
21.(13分) (1分)
⑴(2分)测定pH 或滴加Na2CO3溶液 或将甲酸滴加到滴有酚酞的NaOH溶液中(不能用Na,其它合理答案均可得分)
⑵(2分)测定HCOONa溶液的pH;或将等pH的HCOOH溶液和HCl溶液稀释相同倍数,测其pH的变化;或比较等浓度甲酸和盐酸的导电性等(合理均可给分)
⑶(2分)出现银镜,由于羟基对醛基的影响,导致甲酸中的醛基不具有典型醛基的性质(1分。羧基中C原子和2个O原子之间形成1个大л键,而使甲酸分子中的醛基性质不太典型);或答稀氨水量不足,使甲酸与银氨溶液混合后仍显酸性(1分)
⑷ ① 甲酸在浓硫酸的作用下脱水生成CO和H2O(2分)
 ②(4分)
②(4分)
四.(本题包括3小题,共34分)
22.(9分)(每空各1分)
(1)氮气 ,氮化硅(化学式同样给分)
(2)K=[c(CO)]6/[c(N2)]2
(3)< , 减小,6 mol•L-1.min‑1
(4)升高温度或增大压强 , t3∽t4
(5)50% (3分)
23.(11分)
(1)D (1分)
(2)Cu (1分)
(3)H2 (1分) ;①随着反应进行生成铝离子浓度增大,水解程度增大,产生H+的浓度增大;②该反应放热,升高温度反应加快; ③铜与铝构成原电池,加快铝溶解。(3分)
(4)A、B、D (3分)
(5)A(1分),电解质性质(合理解答同样给分) (1分)
24.(12分)
|