
题目列表(包括答案和解析)
某溶液中含有K+、NH+4、Al3+、OH-、AlO-2、SO2-4、CO2-3、SiO2-3、Cl-等离子中的某几种。现进行如下实验:①取少量溶液逐滴加入盐酸,先无明显现象,当盐酸加到一定体积后开始产生沉淀并逐渐增多,在沉浣不再增加后又产生一种无色气体,在气体不再产生后沉淀开始溶解,直至最后完全消失;
②取①所得溶液,加入Ba(OH)2溶液,无明显现象。
(1)原溶液中肯定存在的离子是 ;肯定不存在的离子是 。
(2)已知用一定体积的原溶液进行实验①时,需消耗0.2 mol/L的盐酸5 mL,这时向所得溶液中加入足量的硝酸银溶液可得沉淀0.187g,则原溶液中 (填“有”“没有”或“不确定”)Cl-。
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图如下:
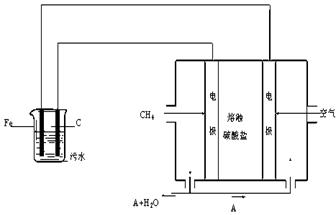
⑴实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的 。
a.H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH
⑵电解池阳极的电极反应分别是① ;
②4OH- - 4 e-= 2H2O + O2↑。
⑶电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是 。
⑷该熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是CH4 + 4CO32- - 8e-= 5CO2 + 2H2O。
①正极的电极反应是 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是 。
⑸实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)___________L。
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图如下:
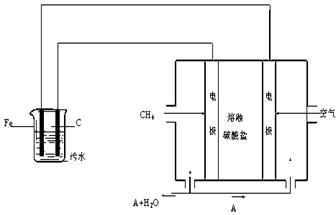
⑴实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的 。
a.H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH
⑵电解池阳极的电极反应分别是① ;
②4OH- - 4 e-= 2H2O + O2↑。
⑶电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是 。
⑷该熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是CH4 + 4CO32- - 8e-= 5CO2 + 2H2O。
①正极的电极反应是 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是 。
⑸实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)___________L。
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图如下:
⑴实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的 。
a.H2SO4 b.BaSO4 c.Na2SO4 d.NaOH e.CH3CH2OH
⑵电解池阳极的电极反应分别是① ;
②4OH- - 4 e-= 2H2O + O2↑。
⑶电极反应①和②的生成物反应得到Fe(OH)3沉淀的离子方程式是 。
⑷该熔融盐燃料电池是以熔融碳酸盐为电解质,以CH4为燃料,空气为氧化剂,稀土金属材料为电极。已知负极的电极反应是CH4 +4CO32- - 8e-= 5CO2 + 2H2O。
①正极的电极反应是 。
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是 。
⑸实验过程中,若在阴极产生了44.8 L(标准状况)气体,则熔融盐燃料电池消耗CH4(标准状况)___________L。
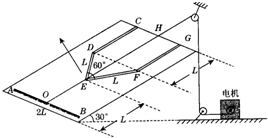 (2011?普陀区二模)如图所示(a),在倾角为300的斜面上固定一光滑金属导轨CDEFG,OH∥CD∥FG,∠DEF=60°,CD=DE=EF=FG=AB/2=L,一根质量为m的导体棒AB在电机的牵引下,以恒定的速度v0沿OH方向从斜面底部开始运动,滑上导轨并到达斜面顶端,AB⊥OH,金属导轨的CD、FG段电阻不计,DEF段与AB棒材料、横截面积均相同,单位长度电阻为r,O是AB棒的中点,整个斜面处在垂直斜面向上磁感应强度为B的匀强磁场中.求:
(2011?普陀区二模)如图所示(a),在倾角为300的斜面上固定一光滑金属导轨CDEFG,OH∥CD∥FG,∠DEF=60°,CD=DE=EF=FG=AB/2=L,一根质量为m的导体棒AB在电机的牵引下,以恒定的速度v0沿OH方向从斜面底部开始运动,滑上导轨并到达斜面顶端,AB⊥OH,金属导轨的CD、FG段电阻不计,DEF段与AB棒材料、横截面积均相同,单位长度电阻为r,O是AB棒的中点,整个斜面处在垂直斜面向上磁感应强度为B的匀强磁场中.求:湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com