
题目列表(包括答案和解析)
 (2008?连云港)图是A、B、C三种固体物质(固体组成与溶质相同)的溶解度曲线.在t1℃时,将质量为a g的A、B、C三种物质分别加入100g水中,根据图示回答下列问题:
(2008?连云港)图是A、B、C三种固体物质(固体组成与溶质相同)的溶解度曲线.在t1℃时,将质量为a g的A、B、C三种物质分别加入100g水中,根据图示回答下列问题:
| 20mL×1.18g/cm3×37% |
| 20mL×1.18g/cm3+60mL×1.0g/cm3 |
| 20mL×1.18g/cm3×37% |
| 20mL×1.18g/cm3+60mL×1.0g/cm3 |
| 实验步骤 | 实验现象和结论 |
分别取等量三种溶液于三支试管中,滴加酚酞试液; 2、向未变红的两支试管中继续滴加鉴别出的氢氧化钠溶液. 分别取等量三种溶液于三支试管中,滴加酚酞试液; 2、向未变红的两支试管中继续滴加鉴别出的氢氧化钠溶液. |
一支试管中溶液变为红色,另外两支不变色.变红的为氢氧化钠溶液; 滴入相同滴数的氢氧化钠,一支试管中的溶液先变成红色,溶液先变红的是溶质质量分数为5%的盐酸,然后继续滴向另外一支继续滴加氢氧化钠溶液后变红.后变红的是溶质质量分数为10%的盐酸. 一支试管中溶液变为红色,另外两支不变色.变红的为氢氧化钠溶液; 滴入相同滴数的氢氧化钠,一支试管中的溶液先变成红色,溶液先变红的是溶质质量分数为5%的盐酸,然后继续滴向另外一支继续滴加氢氧化钠溶液后变红.后变红的是溶质质量分数为10%的盐酸. |
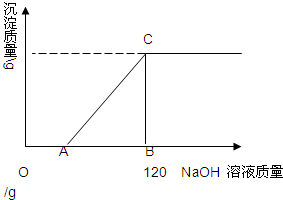 有盐酸和MgCl2的混合溶液共100g,向混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成的沉淀与加入的NaOH溶液质量关系如图所示.若HCl在混合溶液中质量分数为3.65%.求:
有盐酸和MgCl2的混合溶液共100g,向混合溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成的沉淀与加入的NaOH溶液质量关系如图所示.若HCl在混合溶液中质量分数为3.65%.求:湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com