
题目列表(包括答案和解析)
十七、人从哪里来?往哪里去?这是人类永恒的话题……
43.地球的年龄到底有多大?科学家利用天然放射性元素的衰变规律,通过对目前发现的最古老的岩石中铀和铅含量的测定,推算出该岩石中含有的铀是岩石形成初期时的一半。铀238的相对含量随时间变化关系如图示。由此推断,地球的年龄大致为 。
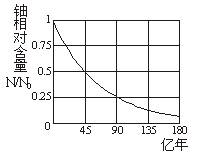
地球为什么会成为生命的摇篮?试分析地球的宇宙环境和地理环境的特点与生命物质存在条件的关系,并用直线相连。
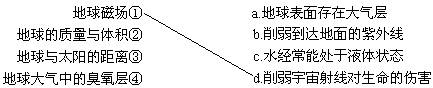
44.生命是如何产生的?米勒曾将水、氨气、甲烷、氢气放在密闭的容器中用电炉加热,同时模拟原始地球电闪雷鸣条件,对其进行长时间放电,最终发现在容器中有简单的氨基酸等有机小分子生成。氨基酸可进一步生成 。这个实验模拟了 的基础物质的形成。
地球生命在外观上千姿百态,但在微观上则基本一致。从微生物到人,遗传物质都是 ,它能在细胞分裂和繁殖过程中正确地 ,保证了生命的延续性。
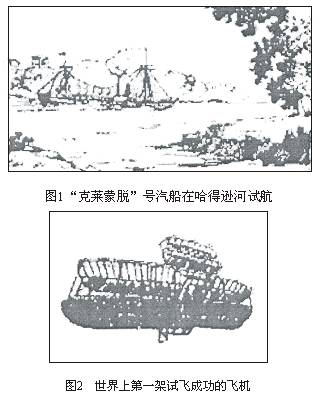
45.从石器时代到信息时代,人类取得了无数重要的科学成果。根据上图,请回答:图1中富尔敦创制的“克莱蒙脱”号汽船运用了瓦特改良的 。图2中飞机的发明者是 。
分析第一次科技革命和第二次科技革命给人类社会带来的共同影响。
46.人类在探索自然规律的进程中总结了许多科学方法。如分析归纳法、演绎法、等效替代法、控制变量法、理想实验法等。在下列研究中,运用理想实验方法进行研究的是( )
A.爱因斯坦提出光子假说
B.查理得出气体状态变化的规律
C.卢瑟福提出原子的核式结构模型
D.伽利略得出力不是维持物体运动原因的结论
现在人们已能合成自然界并不存在的许多性能优良的有机高分子材料,出氯乙烯制取聚氯乙烯的反应属于____反应。
适合于合成聚氯乙烯的原料是( )
A.CH4,Cl2
B.CH3CH3,HCl
C.CH≡CH,HCl
D.CH2==CH2,HCl,
人类在不断探索生命的奥秘,提高生命质量。为了解人类自身的所有基因及其功能,有关国家联合实施了一项 计划。该项研究于2001年初已完成了 测序工作。
47.在漫长的岁月里,人类不断发现、不断创造……。正如马克思主义哲学所认为,人类对客观世界的认识遵循着“实践—认识—实践”不断深化的规律。请在A、B处填写相应内容。
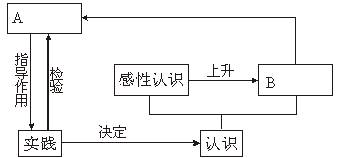
科学技术对社会和经济发展的巨大贡献,日益证明了邓小平同志的科学论断:“ ”。
科学思想、科学精神、科学方法和先进技术引导人类继续在不断的探索中前进……
【选做题】本题包括A、B、C三小题,请选定其中两题,并在答题卡相应的答题区域内作答.若三题都做,则按A、B两题评分.
A.(选修模块3—3)(12分)
(1)利用油酸在水面上形成一单分子层油膜的实验,估测分子直径的大小.有以下的实验步骤:
A、在边长约40cm的浅盘里倒入自来水,深约2cm,将少许痱子粉均匀地轻轻撒在水面上;
B、将5mL的油酸倒入盛有酒精的玻璃杯中,盖上盖并摇动,使油酸均匀溶解形成油酸酒精溶液,读出该溶液的体积为V(mL)
C、用滴管往盘中水面上滴1滴油酸酒精溶液.由于酒精溶于水而油酸不溶于水,于是该滴中的油酸就在水面上散开,形成油酸薄膜;
D、用滴管将油酸酒精溶液一滴一滴地滴人空量杯中,记下当杯中溶液达到1 mL时的总滴数n;
E、取下玻璃板放在方格纸上,量出该单分子层油酸膜的面积S(cm2).
F、将平板玻璃放在浅方盘上,待油酸薄膜形状稳定后可认为已形成单分子层油酸膜.用彩笔将该单分子层油酸膜的轮廓画在玻璃板上.
①完成该实验的实验步骤顺序应该是 ▲ .
②在估算油酸分子直径大小时,可将分子看成球形.用以上实验步骤中的数据和符号表示,油酸分子直径的大小约为d= ▲ cm.
(2)在油膜法测分子直径的实验中,用盆口直径为0.4m的面盆盛水,要让油酸滴在水面上散成单分子的油酸膜,那么油酸体积不能大于多少 ▲ m3,实验中可以先把油酸稀释成油酸溶液,再用特制滴管把这种油酸滴1滴到水面上.若测得1mL油酸溶液为120滴,那么1mL油酸至少应稀释成
▲ mL的油酸溶液.
(3)质量为6.0kg、温度为-20oC的冰全部变成30oC的水,后在常温下(30oC)全部蒸发为水蒸气,整个过程需要吸收多少热量?(设水在常温下的汽化热为L =2.4×106J/kg,冰的比热容为2.1×103J/kgoC,水的比热容为4.2×103J/kgoC,冰的熔化热为![]() =3.34×105J/kg)
=3.34×105J/kg)
B.(选修模块3—4)(12分)
(1)在以下各种说法中,正确的是 ▲
A.一单摆做简谐运动,摆球的运动周期不随摆角和摆球质量的改变而改变
B.光的偏振现象说明光具有波动性,实际上,所有波动形式都可以发生偏振现象.
C.横波在传播过程中,波峰上的质点运动到相邻的波峰所用的时间为一个周期
D.变化的电场一定产生变化的磁场;变化的磁场一定产生变化的电场
E.在光的双逢干涉实验中,若仅将入射光由红光改为绿光,则干涉条纹间距变窄
F.真空中光速在不同的惯性参考系中都是相同的,与光源、观察者间的相对运动没有关系
G.火车过桥要慢行,目的是使驱动力频率远小于桥梁的固有频率,以免发生共振损坏桥梁
H.光导纤维有很多的用途,它由内芯和外套两层组成,外套的折射率比内芯要大
(2)有两个同学利用假期分别去参观北大和南大的物理实验室,各自在那里利用先进的DIS系统较准确地探究了“单摆的周期T与摆长L的关系”,他们通过校园网交换实验数据,并由计算机绘制了T2~L图像,如图甲所示.去北大的同学所测实验结果对应的图线是 ▲ (选填“A”或“B”).另外,在南大做探究的同学还利用计算机绘制了两种单摆的振动图像(如图乙所示),由图可知,两单摆摆长之比![]() ▲ .
▲ .
 |
 (3)如图所示,一截面为正三角形的棱镜,其折射率为
(3)如图所示,一截面为正三角形的棱镜,其折射率为 .今有一束单色光
.今有一束单色光
射到它的一个侧面,经折射后与底边平行,再射向另一侧面后射出.试求
出射光线相对于第一次射向棱镜的入射光线偏离了多少角度?
C.(选修模块3—5)(12分)
(1)下列说法正确的是 ▲
A、太阳辐射的能量主要来自太阳内部的核裂变反应
B、汤姆生发现电子,表明原子具有核式结构
C、一束光照射到某种金属上不能发生光电效应,是因为该束光的波长太短
D、按照玻尔理论,氢原子核外电子从半径较小的轨道跃迁到半径较大的轨道时,电子的动能减小,原子总能量增大
E、E=mc2表明物体具有的能量与其质量成正比
F、 β衰变所释放的电子是原子核内的中子转化成质子和电子所产生的
(2)在光滑的水平面上有甲、乙两个物体发生正碰,已知甲的质量为1kg,乙的质量为3kg,碰前碰后的位移时间图像如图所示,碰后乙的图像没画,则碰后乙的速度大小为 ▲ m/s,碰撞前后乙的速度方向 ▲ (填“变”、“不变”)
(3)从某金属表面逸出光电子的最大初动能![]() 与入射光的频率
与入射光的频率 的图像如下图所示,则这种金属的截止频率是____▲____HZ;普朗克常量是 _▲___Js.
的图像如下图所示,则这种金属的截止频率是____▲____HZ;普朗克常量是 _▲___Js.


【选做题】本题包括A、B、C三小题,请选定其中两题,并在答题卡相应的答题区域内作答.若三题都做,则按A、B两题评分.
A.(选修模块3—3)(12分)
(1)利用油酸在水面上形成一单分子层油膜的实验,估测分子直径的大小.有以下的实验步骤:
A、在边长约40cm的浅盘里倒入自来水,深约2cm,将少许痱子粉均匀地轻轻撒在水面上;
B、将5mL的油酸倒入盛有酒精的玻璃杯中,盖上盖并摇动,使油酸均匀溶解形成油酸酒精溶液,读出该溶液的体积为V(mL)
C、用滴管往盘中水面上滴1滴油酸酒精溶液.由于酒精溶于水而油酸不溶于水,于是该滴中的油酸就在水面上散开,形成油酸薄膜;
D、用滴管将油酸酒精溶液一滴一滴地滴人空量杯中,记下当杯中溶液达到1 mL时的总滴数n;
E、取下玻璃板放在方格纸上,量出该单分子层油酸膜的面积S(cm2).
F、将平板玻璃放在浅方盘上,待油酸薄膜形状稳定后可认为已形成单分子层油酸膜.用彩笔将该单分子层油酸膜的轮廓画在玻璃板上.
①完成该实验的实验步骤顺序应该是 ▲ .
②在估算油酸分子直径大小时,可将分子看成球形.用以上实验步骤中的数据和符号表示,油酸分子直径的大小约为d= ▲ cm.
(2)在油膜法测分子直径的实验中,用盆口直径为0.4m的面盆盛水,要让油酸滴在水面上散成单分子的油酸膜,那么油酸体积不能大于多少 ▲ m3,实验中可以先把油酸稀释成油酸溶液,再用特制滴管把这种油酸滴1滴到水面上.若测得1mL油酸溶液为120滴,那么1mL油酸至少应稀释成
▲ mL的油酸溶液.
(3)质量为6.0kg、温度为-20oC的冰全部变成30oC的水,后在常温下(30oC)全部蒸发为水蒸气,整个过程需要吸收多少热量?(设水在常温下的汽化热为L =2.4×106J/kg,冰的比热容为2.1×103J/kgoC,水的比热容为4.2×103J/kgoC,冰的熔化热为 =3.34×105J/kg)
=3.34×105J/kg)
B.(选修模块3—4)(12分)
(1)在以下各种说法中,正确的是 ▲
A.一单摆做简谐运动,摆球的运动周期不随摆角和摆球质量的改变而改变
B.光的偏振现象说明光具有波动性,实际上,所有波动形式都可以发生偏振现象.
C.横波在传播过程中,波峰上的质点运动到相邻的波峰所用的时间为一个周期
D.变化的电场一定产生变化的磁场;变化的磁场一定产生变化的电场
E.在光的双逢干涉实验中,若仅将入射光由红光改为绿光,则干涉条纹间距变窄
F.真空中光速在不同的惯性参考系中都是相同的,与光源、观察者间的相对运动没有关系
G.火车过桥要慢行,目的是使驱动力频率远小于桥梁的固有频率,以免发生共振损坏桥梁
H.光导纤维有很多的用途,它由内芯和外套两层组成,外套的折射率比内芯要大
(2)有两个同学利用假期分别去参观北大和南大的物理实验室,各自在那里利用先进的DIS系统较准确地探究了“单摆的周期T与摆长L的关系”,他们通过校园网交换实验数据,并由计算机绘制了T2~L图像,如图甲所示.去北大的同学所测实验结果对应的图线是
▲ (选填“A”或“B”).另外,在南大做探究的同学还利用计算机绘制了两种单摆的振动图像(如图乙所示),由图可知,两单摆摆长之比 ▲ .
▲ .
 |
 (3)如图所示,一截面为正三角形的棱镜,其折射率为
(3)如图所示,一截面为正三角形的棱镜,其折射率为 .今有一束单色光
.今有一束单色光
射到它的一个侧面,经折射后与底边平行,再射向另一侧面后射出.试求
出射光线相对于第一次射向棱镜的入射光线偏离了多少角度?
C.(选修模块3—5)(12分)
(1)下列说法正确的是 ▲
A、太阳辐射的能量主要来自太阳内部的核裂变反应
B、汤姆生发现电子,表明原子具有核式结构
C、一束光照射到某种金属上不能发生光电效应,是因为该束光的波长太短
D、按照玻尔理论,氢原子核外电子从半径较小的轨道跃迁到半径较大的轨道时,电子的动能减小,原子总能量增大
E、E=mc2表明物体具有的能量与其质量成正比
F、 β衰变所释放的电子是原子核内的中子转化成质子和电子所产生的
(2)在光滑的水平面上有甲、乙两个物体发生正碰,已知甲的质量为1kg,乙的质量为3kg,碰前碰后的位移时间图像如图所示,碰后乙的图像没画,则碰后乙的速度大小为 ▲ m/s,碰撞前后乙的速度方向 ▲ (填“变”、“不变”)
(3)从某金属表面逸出光电子的最大初动能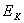 与入射光的频率
与入射光的频率 的图像如下图所示,则这种金属的截止频率是____▲____HZ;普朗克常量是
_▲___Js.
的图像如下图所示,则这种金属的截止频率是____▲____HZ;普朗克常量是
_▲___Js.


第七部分 热学
热学知识在奥赛中的要求不以深度见长,但知识点却非常地多(考纲中罗列的知识点几乎和整个力学——前五部分——的知识点数目相等)。而且,由于高考要求对热学的要求逐年降低(本届尤其低得“离谱”,连理想气体状态方程都没有了),这就客观上给奥赛培训增加了负担。因此,本部分只能采新授课的培训模式,将知识点和例题讲解及时地结合,争取让学员学一点,就领会一点、巩固一点,然后再层叠式地往前推进。
一、分子动理论
1、物质是由大量分子组成的(注意分子体积和分子所占据空间的区别)
对于分子(单原子分子)间距的计算,气体和液体可直接用![]() ,对固体,则与分子的空间排列(晶体的点阵)有关。
,对固体,则与分子的空间排列(晶体的点阵)有关。

【例题1】如图6-1所示,食盐(NaCl)的晶体是由钠离子(图中的白色圆点表示)和氯离子(图中的黑色圆点表示)组成的,离子键两两垂直且键长相等。已知食盐的摩尔质量为58.5×10-3kg/mol,密度为2.2×103kg/m3,阿伏加德罗常数为6.0×1023mol-1,求食盐晶体中两个距离最近的钠离子中心之间的距离。
【解说】题意所求即图中任意一个小立方块的变长(设为a)的![]() 倍,所以求a成为本题的焦点。
倍,所以求a成为本题的焦点。
由于一摩尔的氯化钠含有NA个氯化钠分子,事实上也含有2NA个钠离子(或氯离子),所以每个钠离子占据空间为 v = ![]()
而由图不难看出,一个离子占据的空间就是小立方体的体积a3 ,
即 a3 = ![]() =
= ![]() ,最后,邻近钠离子之间的距离l =
,最后,邻近钠离子之间的距离l = ![]() a
a
【答案】3.97×10-10m 。
〖思考〗本题还有没有其它思路?
〖答案〗每个离子都被八个小立方体均分,故一个小立方体含有![]() ×8个离子 =
×8个离子 = ![]() 分子,所以…(此法普遍适用于空间点阵比较复杂的晶体结构。)
分子,所以…(此法普遍适用于空间点阵比较复杂的晶体结构。)
2、物质内的分子永不停息地作无规则运动
固体分子在平衡位置附近做微小振动(振幅数量级为0.1![]() ),少数可以脱离平衡位置运动。液体分子的运动则可以用“长时间的定居(振动)和短时间的迁移”来概括,这是由于液体分子间距较固体大的结果。气体分子基本“居无定所”,不停地迁移(常温下,速率数量级为102m/s)。
),少数可以脱离平衡位置运动。液体分子的运动则可以用“长时间的定居(振动)和短时间的迁移”来概括,这是由于液体分子间距较固体大的结果。气体分子基本“居无定所”,不停地迁移(常温下,速率数量级为102m/s)。
无论是振动还是迁移,都具备两个特点:a、偶然无序(杂乱无章)和统计有序(分子数比率和速率对应一定的规律——如麦克斯韦速率分布函数,如图6-2所示);b、剧烈程度和温度相关。

气体分子的三种速率。最可几速率vP :f(v) = ![]() (其中ΔN表示v到v +Δv内分子数,N表示分子总数)极大时的速率,vP =
(其中ΔN表示v到v +Δv内分子数,N表示分子总数)极大时的速率,vP =![]() =
=![]() ;平均速率
;平均速率![]() :所有分子速率的算术平均值,
:所有分子速率的算术平均值,![]() =
=![]() =
=![]() ;方均根速率
;方均根速率![]() :与分子平均动能密切相关的一个速率,
:与分子平均动能密切相关的一个速率,![]() =
=![]() =
=![]() 〔其中R为普适气体恒量,R = 8.31J/(mol.K)。k为玻耳兹曼常量,k =
〔其中R为普适气体恒量,R = 8.31J/(mol.K)。k为玻耳兹曼常量,k = ![]() = 1.38×10-23J/K 〕
= 1.38×10-23J/K 〕
【例题2】证明理想气体的压强P = ![]() n
n![]() ,其中n为分子数密度,
,其中n为分子数密度,![]() 为气体分子平均动能。
为气体分子平均动能。

【证明】气体的压强即单位面积容器壁所承受的分子的撞击力,这里可以设理想气体被封闭在一个边长为a的立方体容器中,如图6-3所示。
考查yoz平面的一个容器壁,P = ![]() ①
①
设想在Δt时间内,有Nx个分子(设质量为m)沿x方向以恒定的速率vx碰撞该容器壁,且碰后原速率弹回,则根据动量定理,容器壁承受的压力
F =![]() =
=![]() ②
②
在气体的实际状况中,如何寻求Nx和vx呢?
考查某一个分子的运动,设它的速度为v ,它沿x、y、z三个方向分解后,满足
v2 = ![]() +
+ ![]() +
+ ![]()
分子运动虽然是杂乱无章的,但仍具有“偶然无序和统计有序”的规律,即
![]() =
= ![]() +
+ ![]() +
+ ![]() = 3
= 3![]() ③
③
这就解决了vx的问题。另外,从速度的分解不难理解,每一个分子都有机会均等的碰撞3个容器壁的可能。设Δt = ![]() ,则
,则
Nx = ![]() ·3N总 =
·3N总 = ![]() na3 ④
na3 ④
注意,这里的![]() 是指有6个容器壁需要碰撞,而它们被碰的几率是均等的。
是指有6个容器壁需要碰撞,而它们被碰的几率是均等的。

结合①②③④式不难证明题设结论。
〖思考〗此题有没有更简便的处理方法?
〖答案〗有。“命令”所有分子以相同的速率v沿+x、?x、+y、?y、+z、?z这6个方向运动(这样造成的宏观效果和“杂乱无章”地运动时是一样的),则 Nx =![]() N总 =
N总 = ![]() na3 ;而且vx = v
na3 ;而且vx = v
所以,P = ![]() =
= ![]() =
= =
=![]() nm
nm![]() =
= ![]() n
n![]()
3、分子间存在相互作用力(注意分子斥力和气体分子碰撞作用力的区别),而且引力和斥力同时存在,宏观上感受到的是其合效果。
分子力是保守力,分子间距改变时,分子力做的功可以用分子势能的变化表示,分子势能EP随分子间距的变化关系如图6-4所示。
分子势能和动能的总和称为物体的内能。
二、热现象和基本热力学定律
1、平衡态、状态参量
a、凡是与温度有关的现象均称为热现象,热学是研究热现象的科学。热学研究的对象都是有大量分子组成的宏观物体,通称为热力学系统(简称系统)。当系统的宏观性质不再随时间变化时,这样的状态称为平衡态。
b、系统处于平衡态时,所有宏观量都具有确定的值,这些确定的值称为状态参量(描述气体的状态参量就是P、V和T)。
c、热力学第零定律(温度存在定律):若两个热力学系统中的任何一个系统都和第三个热力学系统处于热平衡状态,那么,这两个热力学系统也必定处于热平衡。这个定律反映出:处在同一热平衡状态的所有的热力学系统都具有一个共同的宏观特征,这一特征是由这些互为热平衡系统的状态所决定的一个数值相等的状态函数,这个状态函数被定义为温度。
2、温度
a、温度即物体的冷热程度,温度的数值表示法称为温标。典型的温标有摄氏温标t、华氏温标F(F = ![]() t + 32)和热力学温标T(T = t + 273.15)。
t + 32)和热力学温标T(T = t + 273.15)。
b、(理想)气体温度的微观解释:![]() =
= ![]() kT (i为分子的自由度 = 平动自由度t + 转动自由度r + 振动自由度s 。对单原子分子i = 3 ,“刚性”〈忽略振动,s = 0,但r = 2〉双原子分子i = 5 。对于三个或三个以上的多原子分子,i = 6 。能量按自由度是均分的),所以说温度是物质分子平均动能的标志。
kT (i为分子的自由度 = 平动自由度t + 转动自由度r + 振动自由度s 。对单原子分子i = 3 ,“刚性”〈忽略振动,s = 0,但r = 2〉双原子分子i = 5 。对于三个或三个以上的多原子分子,i = 6 。能量按自由度是均分的),所以说温度是物质分子平均动能的标志。
c、热力学第三定律:热力学零度不可能达到。(结合分子动理论的观点2和温度的微观解释很好理解。)
3、热力学过程
a、热传递。热传递有三种方式:传导(对长L、横截面积S的柱体,Q = K![]() SΔ
SΔ
一、选择题:
1. C 2.B 3.D 4.B 5.A 6.C 7.A 8.C 9.C 10.A
11. D 12.B 13.B 14.C 15.BC 16.A 17.BD 18.ABC 19.D 20.BCD
21.D
二、非选择题:t
22.(1)每空2分 计6分
相邻相等时间间隔内的位移差(或△s)相等 匀加速直线运动3.5
(2)①连线正确得4分,电路设计错误得0分,设计正确,连线错误得2分
②U,I,L,d(3分) ③h= (3分)
(3分)
23.O→B
(1)h= .t3=
.t3= …………5分
…………5分
(2)B→A v0=gt g=
g= =3.56(m/s2) …………5分
=3.56(m/s2) …………5分
(3)O→B F-mg=ma ① …………2分
vB=at1 ② …………2分
F=m( )=1.5×103(
)=1.5×103( )=1.63×104(N) …………3分
)=1.63×104(N) …………3分
24.(1)在D点处
F=Bqv1 ① …………2分
FN-mg-F=0 ② …………2分
A→D:mv0=Mv2+mv1 ③ …………3分
△E= ④ …………3分
④ …………3分
解①②③④得△E=18J …………2分
(2)m再次回到D点时M有最大速度
mv1+Mv2=mv3+Mv4 ⑤ …………3分
 ⑥ …………2分
⑥ …………2分
解①②③④⑤⑥可得 v4=3(m/s) …………2分
25.(1) x ① …………2分
x ① …………2分
Ek= ② …………2分
② …………2分
解①②得 Ek= …………2分
…………2分
(2)Uc=ε= =kπr2 ③ …………2分
=kπr2 ③ …………2分
当k有极小值时: ④ …………2分
④ …………2分
解③④得:Kmin= …………2分
…………2分
当k有极大值时: ⑤ …………2分
⑤ …………2分
 ⑥ …………2分
⑥ …………2分
解③⑤⑥得:Kmax= …………2分
…………2分
∴ …………2分
…………2分
26.H+、Cl-,Na+、OH-,NH4Cl,NH4Cl,NH4Cl、NH3?H2O,NH4Cl、HCl
27.(1)MnO2>Cl2>H2O2>H2SO4(或X>C>B>D)
(2)H∶ ∶
∶
(3)Cu+2H2SO4(浓) CuSO4+2H2O+SO2↑ H2O2+Cl2=2HCl+O2
CuSO4+2H2O+SO2↑ H2O2+Cl2=2HCl+O2
(4)SO2+2H2O+Cl2=4H++SO 2Cl-
2Cl-
(5)A、B(3分)
28.(1)b c e a
(2)①反应放热,使溶液温度升高,反应速率增大,
②产生的气体将酸液压到‘U’型管右边,使酸液与Cu丝脱离
(3)‘U’型管左端产生无色气体形成一段气柱,无色气体变为红棕色
(4)①2NO+O2=2NO2,3NO2+H2O=2HNO3+NO
或4NO+3O2+2H2O=4HNO3(4分) ②mol/L ③19
29.(1)C (2)BC (3)酯化、消失、聚合(或缩聚)



 CHCOOH CHO
CHCOOH CHO

 (4)
(4)
OH CHOHCH2OH

 CHO COONH4
CHO COONH4


 (5)
+2Ag(NH3)2OH
(5)
+2Ag(NH3)2OH +2Ag↓+
+2Ag↓+
 CHOHCH2OH CHOHCH2OH
CHOHCH2OH CHOHCH2OH
3NH3+H2O …………3分
注:26~29题中未注明分值的空格,每空2分
30.(21分)
(1)将从S型活细菌中提取出的DNA、蛋白质和多糖等物质,分别加入已培养了R型细菌的培养基中,培养并观察菌落的情况。(4分)
(2)①已灭活的病原微生物体内的抗原物质仍能引起机体的免疫反应(4分)
②体液免疫(2分)
(3)①注射外源抗体可使机体获得一定的免疫能力(3分)
②第二步:选取数只相似的小白鼠,分成数量相等的A、B两组,A组先注射免疫血清,再注射破伤风外毒素,B组内注射破伤风外毒素。(6分)
③A组小鼠正常生活,B组小鼠死亡(2分)
31.(21分)
CH2―CH2―COOH
 |
 (1)H2N―C―COOH (2分); GAG(2分)
(1)H2N―C―COOH (2分); GAG(2分)
H
(2)异养需氧型(2分) 溶氧不足(或通气量不足)(2分)
(3)步骤:菌种的选取、培养基的配制、灭菌、扩大培养(4分)时期:稳定期(2分)
特点:菌体的出生率等于死亡率,且活菌数目达到最大,细胞内大量积累代谢产物,特别是次级代谢产物(4分)
(4)原因:①保证微生物对营养物质的需求;②排出部分有害代谢产物;③使微生物保持较长时间的快速生长.(答一点即可)(3分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com