
题目列表(包括答案和解析)
研究化学反应原理对于生产生活是很有意义的。
(1)下列关于醋酸的叙述正确的是 (填写符号)。
a.等体积等pH的醋酸和盐酸完全被NaOH溶液中和,消耗NaOH的物质的量一样多
b.向醋酸溶液中加入一定量NaOH固体,溶液的导电性增强
c.加水稀释醋酸溶液,溶液中的所有离子浓度均减小
d.常温下,醋酸溶液中水的电离程度比纯水的小
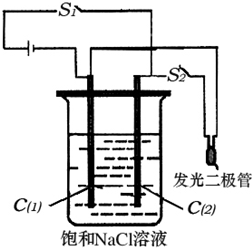
(2)钢铁生锈现象随处可见,钢铁的电化腐蚀原理如图所示:
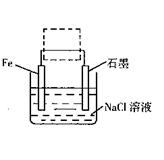
①写出石墨电极的电极反应式 ;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改。
③写出修改后石墨电极的电极反应式 。
(3)①高炉炼铁过程中会发生反应:FeO(s)+CO(g)![]() Fe(s)+CO2(g)。
Fe(s)+CO2(g)。
已知:Fe(s)+1/2O2(g)=FeO(s)△H= -272kJ·mol-1
C(s)+O2(g)=CO2(g) △H= -393.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H= -22lkJ·mol-1
则:①FeO(s)+CO(g)![]() Fe(s)+CO2(g)
Fe(s)+CO2(g)
△H= 。
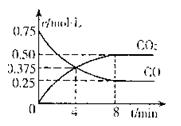
②一定温度下,向某密闭容器中加人足量FeO,
并充人一定量的CO气体,反应过程中CO和CO2的
浓度与时间的关系如图所示则从开始至达到平衡过程中,![]() (CO)= 。
(CO)= 。
(4)铁红是一种红色颜料,其成份是Fe2O3。将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加人一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为 。
研究化学反应原理对于生产生活是很有意义的。
(1)下列关于醋酸的叙述正确的是 (填写符号)。
a.等体积等pH的醋酸和盐酸完全被NaOH溶液中和,消耗NaOH的物质的量一样多
b.向醋酸溶液中加入一定量NaOH固体,溶液的导电性增强
c.加水稀释醋酸溶液,溶液中的所有离子浓度均减小
d.常温下,醋酸溶液中水的电离程度比纯水的小
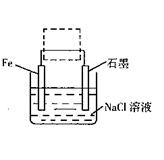
(2)钢铁生锈现象随处可见,钢铁的电化腐蚀原理如图所示:
①写出石墨电极的电极反应式 ;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在右图虚线框内所示位置作出修改。
③写出修改后石墨电极的电极反应式 。
(3)①高炉炼铁过程中会发生反应:FeO(s)+CO(g) Fe(s)+CO2(g)。
Fe(s)+CO2(g)。
已知:Fe(s)+1/2O2(g)=FeO(s)△H= -272kJ·mol-1
C(s)+O2(g)=CO2(g) △H= -393.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H= -22lkJ·mol-1
则:①FeO(s)+CO(g) Fe(s)+CO2(g)
Fe(s)+CO2(g)
△H= 。
②一定温度下,向某密闭容器中加人足量FeO,
并充人一定量的CO气体,反应过程中CO和CO2的
浓度与时间的关系如图所示则从开始至达到平衡过程中, (CO)= 。
(CO)= 。
(4)铁红是一种红色颜料,其成份是Fe2O3。将一定量的铁红溶于160mL 5mol·L-1盐酸中,再加人一定量铁粉恰好完全溶解,收集到气体2.24L(标准状况),经检测,溶液中无Fe3+,则参加反应的铁粉的质量为 。
 Fe(s)+CO2(g)。
Fe(s)+CO2(g)。 Fe(s)+CO2(g)
Fe(s)+CO2(g)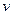 (CO)= 。
(CO)= 。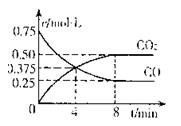
 (1)现有如下两个反应:
(1)现有如下两个反应:
| ||
| ||
(9分)工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。
(1)某温度下,SO2(g)+1/2O2(g)![]() SO3(g);△H==-98kJ/mol。开始时在100L的密闭容器中加
SO3(g);△H==-98kJ/mol。开始时在100L的密闭容器中加
入4.0molSO2(g)和10.0molO2(g),当反应达到平衡时共放出热量196kJ,该温度下平衡常数
K=____________________
(2)一定条件下,向一带有活塞的密闭容器中充入2molSO2(g)和1molO2(g),发生下列反应:
2SO2(g)+O2(g)![]() 2SO3(g)达到平衡后改变下列条件,SO2、O2、SO3气体平衡浓度都比原来增
2SO3(g)达到平衡后改变下列条件,SO2、O2、SO3气体平衡浓度都比原来增
大的是____________(填字母)。
A.保持温度和容器体积不变,充入2molSO3 B.保持温度和容器体积不变,充入2molN2
C.保持温度和容器体积不变,充入0.5molSO2和0.25molO2
D.保持温度和容器内压强不变,充入1molSO3
E.升高温度 F.移动活塞压缩气体
(3)某人设想以右图所示装置用电化学原理生产硫酸,写出通入
SO2的电极的电极反应式:_____________
(4)若通入SO2的速率为2.24L/min(标准状况),为稳定
持续生产,硫酸溶液的浓度应维持不变,则左侧水的流
入速率应为_______________mL/min。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com