¹¤̉µºÏ³É°±ÓëÖƱ¸ÏơËá̉»°ă¿ÉÁ¬ĐøÉú²ú£¬Á÷³̀ÈçÏÂ
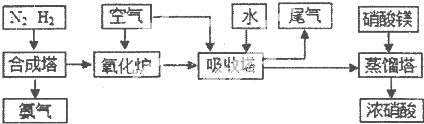
£¨1£©¢Ù¹¤̉µÉú²úʱ£¬ÖÆÈ¡ÇâÆøµÄ̉»¸ö·´Ó¦Îª£ºCO+H
2O£¨g£©?CO
2+H
2£¬850¡æʱ£¬Íù1LĂܱƠÈƯÆ÷ÖĐ³äÈë0.3mol COºÍ0.2molH
2O£¨g£©£®·´Ó¦4minºó½¨Á¢Æ½ºâ£¬̀åϵÖĐc£¨H
2£©=0.12mol?L
-1£®COµÄƽºâŨ¶ÈΪ
0.18mol/L
0.18mol/L
ת»¯ÂÊΪ
40%
40%
¸ĂζÈÏ´˷´Ó¦µÄƽºâ³£ÊưK=
1
1
£῭î¼ÆËă½á¹û£©£®
¢ÚÔÚ850¡æʱ£¬̉Ô±íÖеÄÎïÖʵÄÁ¿Í¶ÈëºăÈƯ·´Ó¦Æ÷ÖĐ£¬ÆäÖĐỊ̈Äæ·´Ó¦·½Ị̈½øĐеÄÓĐ
A
A
£¨Ñ¡̀îA¡¢B¡¢C¡¢D¡¢E£©
|
A |
B |
C |
D |
E |
| n£¨CO2£© |
3 |
l |
0 |
1 |
l |
| n£¨H2£© |
2 |
l |
0 |
1 |
2 |
| n£¨CO£© |
1 |
2 |
3 |
0.5 |
3 |
| n£¨H2O£© |
5 |
2 |
3 |
2 |
l |
£¨2£©ºÏ³ÉË₫ÖĐ·¢Éú·´Ó¦N
2£¨g£©+3H
2£¨g£©?2NH
3£¨g£©¡÷H£¼0£®Ï±íΪ²»Í¬Î¶Èϸ÷´Ó¦µÄƽºâ³£Êư£®ÓÉ´Ë¿ÉÍÆÖª£¬±íÖĐT
1£¼
£¼
300¡æ£῭î¡°£¾¡±¡¢¡°£¼¡±»̣¡°=¡±£©£®
| T/¡ăC |
T1 |
300 |
T2 |
| K |
1.00¡Á107 |
2.45¡Á105 |
1.88¡Á103 |
£¨3£©N
2ºÍH
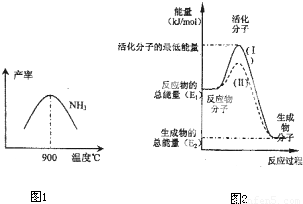
2ÔÚ̀ú×÷´ß»¯¼Á×÷ÓĂÏ´Ó145¡æ¾Í¿ªÊ¼·´Ó¦£¬²»Í¬Î¶ÈÏÂNH
3²úÂÊͼ1Ëùʾ£®Î¶ȸßÓÚ900¡æʱ£¬NH
3²úÂÊϽµ£¬Ộ̉ÊÇ
900¡æʱ·´Ó¦´ïµ½Æ½ºâ×´̀¬£¬ÔÙÉư¸ßζÈƽºâỊ̈×ó̉ƶ¯
900¡æʱ·´Ó¦´ïµ½Æ½ºâ×´̀¬£¬ÔÙÉư¸ßζÈƽºâỊ̈×ó̉ƶ¯
£®
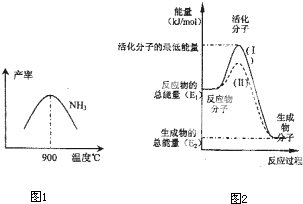
£¨4£©ÔÚ»¯Ñ§·´Ó¦ÖĐÖ»ÓĐ¼«ÉÙÊưÄÜÁ¿±Èƽ¾ùÄÜÁ¿¸ßµĂ¶àµÄ·´Ó¦Îï·Ö×Ó·¢ÉúÅöײʱ²Å¿ÉÄÜ·¢Éú»¯Ñ§·´Ó¦£¬ƠâĐ©·Ö×Ó±»³ÆΪ»î»¯·Ö×Ó£®Ê¹ÆƠͨ·Ö×Ó±ä³É»î»¯·Ö×ÓËùĐè̀ṩµÄ×îµÍÏ̃¶ÈµÄÄÜÁ¿½Đ»î»¯ÄÜ£¬Æ䵥λͨ³£ÓĂkJ?mol
-1±íʾ£®ÇëÈÏƠæ¹Û²́ͼ2£¬»Ø´đÎỀ⣮
ͼÖĐËùʾ·´Ó¦ÊÇ
·ÅÈÈ
·ÅÈÈ
£῭î¡°ÎüÈÈ¡±»̣¡°·ÅÈÈ¡±£©·´Ó¦£¬¸Ă·´Ó¦µÄ¡÷H=
-£¨E1-E2£©kJ/mol
-£¨E1-E2£©kJ/mol
£¨ÓĂº¬E
1¡¢E
2EµÄ´úÊưʽ±íʾ£©£®̉ÑÖªÈÈ»¯Ñ§·½³̀ʽ£ºH
2£¨g£©+
O
2£¨g£©=H
2O£¨g£©¡÷H=-241.8kJ?mol
-1£¬¸Ă·´Ó¦µÄ»î»¯ÄÜΪ167.2kJ?mol
-1£¬ỘÆäÄæ·´Ó¦µÄ»î»¯ÄÜΪ
409kJ/mol
409kJ/mol
£®
£¨5£©ÏơË᳧µÄβÆøÖ±½ÓÅŷŽ«ÎÛȾ¿ƠÆø£®Ä¿Ç°¿Æѧ¼̉̀½Ë÷ÀûÓĂȼÁÏÆø̀åÖĐµÄ¼×ÍéµÈ½«µªµÄÑơ»¯ÎﻹÔΪµªÆøºÍË®£¬·´Ó¦»úÀíΪ£º
CH
4£¨g£©+4NO
2£¨g£©=4NO£¨g£©+CO
2£¨g£©+2H
2O£¨g£©¡÷H=-574kJ?mol
-1CH
4£¨g£©+4NO£¨g£©=2N
2£¨g£©+CO
2£¨g£©+2H
2O£¨g£©¡÷H=-1160kJ?mol
-1Ộ¼×ÍéÖ±½Ó½«NO
2»¹ÔΪN
2µÄÈÈ»¯Ñ§·½³̀ʽΪ£º
CH4£¨g£©+2NO2£¨g£©=CO2£¨g£©+2H2O£¨g£©+N2£¨g£©¡÷H=-867kJ?mol-1
CH4£¨g£©+2NO2£¨g£©=CO2£¨g£©+2H2O£¨g£©+N2£¨g£©¡÷H=-867kJ?mol-1
£®




 O2£¨g£©=H2O£¨g£©¡÷H=-241.8kJ?mol-1£¬¸Ă·´Ó¦µÄ»î»¯ÄÜΪ167.2kJ?mol-1£¬ỘÆäÄæ·´Ó¦µÄ»î»¯ÄÜΪ £®
O2£¨g£©=H2O£¨g£©¡÷H=-241.8kJ?mol-1£¬¸Ă·´Ó¦µÄ»î»¯ÄÜΪ167.2kJ?mol-1£¬ỘÆäÄæ·´Ó¦µÄ»î»¯ÄÜΪ £®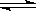 2NH3(g) ¡÷H=£92£®4kJ/mol
2NH3(g) ¡÷H=£92£®4kJ/mol 2NH3(g) ¡÷H=£92£®4kJ/mol
2NH3(g) ¡÷H=£92£®4kJ/mol