
题目列表(包括答案和解析)
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +H2O
+H2O![]() NH3·H2O+H+ ②
NH3·H2O+H+ ②
H++OH-![]() H2O ③
H2O ③
由于![]() 水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解;
乙同学的解释是
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +OH-
+OH-![]() NH3·H2O ②
NH3·H2O ②
由于NH4Cl电离出的![]() 与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
与Mg(OH)2电离出的OH-结合,生成了弱的电解质NH3·H2O,导致反应①的平衡右移,Mg(OH)2沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂,来证明甲、乙两位同学的解释只有一种正确,他选用的试剂是_________(填写编号)。
A.NH4NO3 B.CH3COONH4 C.Na2CO3 D.NH3·H2O
(2)你说明丙同学做出该选择的理由:______________________________。
(3)丙同学将所选试剂滴入Mg(OH)2的浊液中,Mg(OH)2溶解;由此推知,甲和乙哪位同学的解释更合理_____________(填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式_____________________________________。
(12分)几种中学化学常见的单质及其化合物相互转化的关系图如下:
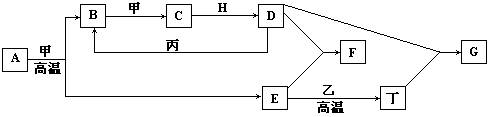 |
可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1:2,元素质量之比为7:8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为 ,每反应1mol的A转移的电子数为 mol;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式: ;
(3)少量F的饱和溶液与分别滴加到下列物质中,得到三种分散系①、②、③。
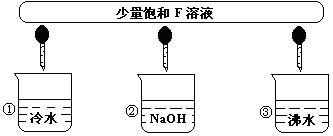 |
试将①、②、③填入下列方框中:
 |
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式: ;
(5)已知丙单质与D的浓溶液按物质的量为1:2恰好反应生成B气体的化学转化式为:
丙 + D(浓)![]() B↑+ 丙的氧化产物 + 水
B↑+ 丙的氧化产物 + 水
则丙在其氧化产物中的化合价为: 。
几种中学化学常见的单质及其化合物相互转化的关系图如下: 
可供参考的信息有:
①甲、乙、丙、丁为单质,其余为化合物
②A由X和Y两种元素组成,其原子个数比为l︰2,元素质量之比为7︰8。
③B气体是引起酸雨的主要物质,H常温下为无色无味的液体,E常用作红色油漆和涂料。
试根据上述信息回答下列问题:
(1)A的化学式为 ,每反应lmol的A转移的电子数为 mol;
(2)F与丁单质也可以化合生成G,试写出该反应的离子方程式: ;
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①、②、③。
试将①、②、③填人下列方框中:
(4)化合物M与H组成元素相同,可以将G氧化为F,且不引进新的离子。试写出M在酸性环境下将G氧化为F的离子方程式: 。
 Mg2++2OH-①
Mg2++2OH-①  NH3·H2O+H+②
NH3·H2O+H+② H2O③
H2O③ Mg2++2OH-①
Mg2++2OH-① NH3·H2O②
NH3·H2O② 甲同学的解释是:
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +H2O
+H2O![]() NH3·H2O+H+ ②
NH3·H2O+H+ ②
H++OH-![]() H2O ③
H2O ③
由于![]() 水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解。
水解显酸性,H+与OH-反应生成水,导致反应①平衡右移,沉淀溶解。
乙同学的解释是:
Mg(OH)2(s)![]() Mg2++2OH- ①
Mg2++2OH- ①
![]() +OH-
+OH-![]() NH3·H2O ②
NH3·H2O ②
由于NH4Cl电离出的![]() 与Mg(OH)2电离出的OH-结合,生成了弱电解质NH3·H2O,导致反应①平衡右移,沉淀溶解。
与Mg(OH)2电离出的OH-结合,生成了弱电解质NH3·H2O,导致反应①平衡右移,沉淀溶解。
(1)丙同学不能肯定哪位同学的解释合理,于是选用下列的一种试剂来证明甲、乙两位同学的解释只有一种正确,他选用的试剂是________(填写编号)。
A.NH4NO3 B.CH3COONH4 C.Na2CO3 D.NH3·H2O
(2)请你说明丙同学作出该选择的理由_____________________________________。
(3)丙同学将所选试剂滴入Mg(OH)2的悬浊液中,Mg(OH)2溶解,由此推知:甲和乙哪位同学的解释更合理_________(填“甲”或“乙”);完成NH4Cl饱和溶液使Mg(OH)2悬浊液溶解的离子方程式___________________________。
选择题
题号
1
2
3
4
5
6
7
8
答案
B
B
C
B
A
C
C
A
题号
9
10
11
12
13
14
15
16
答案
D
BC
AC
D
BC
A
A
C
17、(共8分、每空2分) (1)BD (2)碱式滴定管 (3)量筒 环形玻璃棒
18.(共20分)(1)浓盐酸的浓度随着反应的进行变稀以后,将不再反应(2分);加热时浓盐酸因挥发而损失(2分)
(2)① 无水硫酸铜(2分) 证明有水蒸气产生(2分)
白色变蓝色(其它合理答案也给分)(2分)②氯气无漂白性,次氯酸有漂白性 (2分)③吸收氯气(2分) ④Ag-+Cl-=AgCl↓(2分)
(3)F G(2分) 湿润的淀粉KI试纸(或湿润的有色布条)(2分)
19.(每空2分、共8分)(1)+1
(2)CuI 0.5
(3) 2 Cu2+
+ 5 I ―― 2 CuI + 1 I
―― 2 CuI + 1 I
20. (10分)
(1) Al2O3 ,Cl2
(2) 第三周期第ⅢA族
(3) Al(OH)3 + NaOH = NaAlO2 + 2H2O
(4)在常温下,铝的表面被浓硝酸钝化,生成一薄层致密、坚固的氧化物保护膜,从而阻止内部的金属继续与浓硝酸发生反应。所以铝不溶于冷的浓硝酸。
21、(10分)(1) (2分) 放热(2分)
(2分) 放热(2分)
(2)b、c (2分)
(3)不 (2分)
|