
题目列表(包括答案和解析)
下列有某兴趣小组研究浓硫酸的氧化性的结论并进行了实验验证:
①一般认为1:1的硫酸浓度大于60%,就具有一定的氧化性,越浓氧化性越强,60%以下的H2SO4氧化性就不怎么强了。
②温度也影响氧化性,如铜放于冷的浓硫酸中反应不明显,如果加热就可以观察到明显现象。
③98%的浓硫酸物质的量浓度为18.4mol?L-1,密度为1.84g?cm-3
据以上信息回答:
(1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓硫酸10―15滴(约0.5mL),加热至沸腾,该试管中液体是否有明显变化 。(填“是”或“否”)
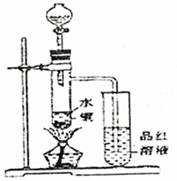
(2)甲同学再用分液漏斗加浓硫酸10mL后加热至沸腾,现象是 。
(3)乙同学利用所示装置直接从分液漏斗中加浓硫酸10mL与铜片反应。所观察到与甲不同的现象是 。为了最终看到与甲类似的现象,乙同学需进行的操作是: 。
(4)乙同学进行加热,还在带支管的试管中观察到有黑色物质出现,大胆假设此物质是
。
下列是某兴趣小组研究浓硫酸的氧化性的结论并进行了实验验证:
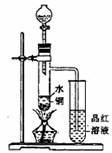
①一般认为1:1的硫酸浓度大于60%,就具有一定的氧化性,越浓氧化性越强,60%以下的H2SO4氧化性就不怎么强了。
②温度也影响氧化性,如铜放于冷的浓硫酸中反应不明显,如果加热就可以观察到明显现象。
③98%的浓硫酸物质的量浓度为18.4mol?L-1,密度为1.84g?cm-3据以上信息回答:
(1)如图装置,同学甲先向带支管的试管中放入铜粉和3mL水,然后从分液漏斗中加98%的浓硫酸10―15滴(约0.5mL),加热至沸腾,该试管中液体是否有明显变化 _____。试用数据解释原因_________________________________。
(2)甲同学再用分液漏斗加浓硫酸10mL再加热至沸腾,现象是_____________________
__________________________。
(3)乙同学利用所示装置直接从分液漏斗中加浓硫酸10mL与铜片反应。所观察到与甲不同的现象是______ ___________________原因是___________ _________________。为了最终看到与甲类似的现象,乙同学需进行的操作是_______________________________________。
(4)乙同学进行加热,还在带支管的试管中观察到有黑色物质出现,大胆假设此物质是_______________。
 下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:
下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:根据下图回答问题:
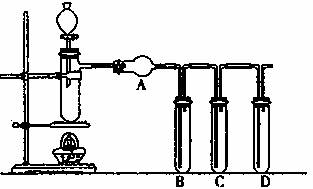
(1)装置气密性的检验须在盛放药品前进行。在上述装置中,往试管B、C、D中各加入5 mL 蒸馏水封住导管口,各连接处都紧密而不漏气的情况下,点燃酒精灯,微热带支管的试管一会儿,试管B、C、D中未出现气泡;熄灭酒精灯后,试管B、C、D中导管内水面也未上升,其原因是: 。
(2)①一般来说,硫酸的质量分数大于60 %,就具有一定的氧化性,且越浓氧化性越强;②温度也要影响氧化性,如铜放于冷的浓硫酸中反应不明显,加热就可观察到明显现象。甲同学利用上述装置,用实验来验证硫酸氧化性的上述结论(已知98%的浓硫酸的密度为1.84g.m-3)。他先向试管B 加人5mL 品红试液,向试管C、D 中各加人5mL饱和澄清石灰水;向带支管的试管中放人铜粉和3mL水,然后从分液漏斗向支管试管中滴加98%的浓硫酸10滴(约0.5mL),加热至沸腾,这时支管试管中溶液颜色是否有明显变化 (填“无”或“有”),试用数据解释其原因 。
该同学用分液漏斗再向支管试管中加98%的浓硫酸10mL,并加热至沸腾,观察到的现象分别是:支管试管中 ,B试管中 。
(3)乙同学利用上述装置来检验浓硫酸和木炭粉在加热条件下发生反应的全部产物
①装置A中应加入的试剂是 。
②装置B、C和D中所加试剂分别是 (填字母序号)
A.澄清石灰水、品红溶液、高锰酸钾酸性溶液
B.品红溶液、高锰酸钾酸性溶液、澄清石灰水
C.高锰酸钾酸性溶液、品红溶液、澄清石灰水
D.澄清石灰水、高锰酸钾酸性溶液、品红溶液
③实验时为了确保D所验证的结论正确,C中应观察到的现象是 。
(4)有同学认为可利用上述装置完成了Cl2的漂白性,氧化性的实验验证,你认为装置A、B、C所加试剂或物品最有可能的分别是 、 、 ;另有同学认为上述装置完成此实验,最好还应加上一个装置,你认为此装置的作用是 。
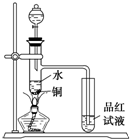 下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:
下面是某化学课外活动小组研究浓H2SO4的氧化性的结论并进行了实验验证:题序
6
7
8
9
10
11
12
答案
D
C
B
B
A
A
B
23.(共15分)
(1)i 从上到下,原子半径增大,失去电子越来越容易
(2)VIII;2 (3)大于
(4) Be2++2OH-=Be(OH)2↓ Be2++4OH-=BeO22-+2H2O
(5)PbO2+4HCl=PbCl2+Cl2 ↑+2H2O
24.(共14分,每空2分)
(1)FeSO3 铁红
(2)气态X的电子式略 极性 共价
(3)SO2+C12+2H2O=4H++SO42-+
25(共16分,每空2分)
(1)否 硫酸溶质质量分数为23%<60%,其氧化性不突出所以无明显现象
(2)铜片慢慢溶解,带支管的试管中溶液渐成蓝色小试管中品红褪色。化学方程式为:Cu+2H2SO4.files/image044.gif) CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
(3)现象是: ①液体呈浅蓝色,原因是溶液中含有Cu2+;②有白色固体在试管底部析出,
原因是:98%浓H2SO4有吸水性只剩无水CuSO4。
操作是:带支管的试管中的溶液冷却后沿烧杯壁缓缓加入到水中,并不断用玻璃棒拌。
30. A.(13分)
(1)C<O<N (2)三角锥形
(3).files/image046.jpg) N2O
N2O
(4)1s22s22p63s23p63d54s1(或[Ar] 3d54s1) [Cr(NH3)4(H2O)2]Cl3
(5)4Mg+10HNO3=4Mg(NO3)2+NH4NO3+3H2O
31(共13分)
(1)CH2ClCHBrCH2Br
.files/image047.gif) CH2OOCCH3
CH2OOCCH3
.files/image048.gif) CHOOCCH3
CHOOCCH3
CH2OOCCH3
(2)a; b c
|