
题目列表(包括答案和解析)
下表是四种盐在不同温度下的溶解度(g/100g水):
|
|
NaNO3 |
KNO3 |
NaCl |
KCl |
|
10℃ |
80.5 |
21.2 |
35.7 |
31.0 |
|
100℃ |
175 |
246 |
39.1 |
56.6 |
(假设:盐类共存时不影响各自的溶解度,分离晶体时,溶剂的损耗忽略不计)
某同学设计用物质的量之比为1∶1的硝酸钠和氯化钾为原料,加入一定量的水制取硝酸钾的实验,其流程如下图所示:
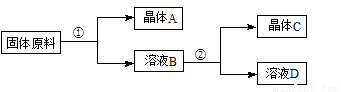
(1)在①和②的实验过程中,需要控制的关键的实验条件是______________________,在上述晶体中,______(填“A”或“C”)应为硝酸钾晶体。
(2)在①的实验过程中,需要进行的操作依次是________________、________________、_____________。
(3)粗产品中可能含有杂质离子_______________________,检验其中一种离子的方法是________________________________________________________________________。
(4)为了洗涤所得的硝酸钾晶体,下列溶剂可用作洗涤剂的是___________(填编号)。
a.热水 b.冰水 c.95%的酒精 d.四氯化碳
(5)如取34.0g硝酸钠和29.8g氯化钾,加入70g水,在100℃蒸发掉50g水,维持该温度,过滤,析出晶体的质量为_______________。
温度/℃ | NaNO3 | KNO3 | NaCl | KCl |
10 | 80.5 | 20.9 | 35.7 | 31.0 |
100 | 175 | 246 | 39.1 | 56.6 |
(假设:①盐类共存时不影响各自的溶解度;②分离晶体时,溶剂的损耗忽略不计)

某同学设计用物质的量比为1∶1的硝酸钠和氯化钾原料,加入一定量的水制取硝酸钾的实验,其流程如上图所示。
(1)在①和③的实验过程中,关键的实验条件是____________________________________。
(2)分离晶体的②和④的操作是_______________(填“倾倒”“蒸发”“结晶”或“过滤”中的某种操作),硝酸钾是晶体_______________(填“A”或“C”)。
(3)粗产品中可能含有的杂质离子是_____________,检验方法是_____________________
____________________________________________________________________。
(4)欲将粗产品提纯,可采取的方法是_____________________________________。


某化学兴趣小组欲从NaNO3和KCl的混合溶液中分离出KNO3,设计了如下实验方案:
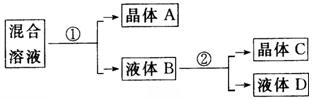
假设:①混合溶液中,n(KCl)=n(NaNO3);②盐类共存时不影响各自的溶解度。溶液中各种溶质在100℃和10℃的溶解度参照例题。试回答下列问题:
(1)①的主要操作是 ;
②的主要操作是 。
(2)晶体A的主要成分是____________,若含有杂质可能是____________。晶体C的主要成分是____________,若含有杂质可能____________;通过实验确定晶体C中是否含有该杂质的方法是 。
(3)若晶体C中确实含有杂质,进一步提纯的方法是____________。
 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应和答题区域内作答.若两题都做,则按A题评分.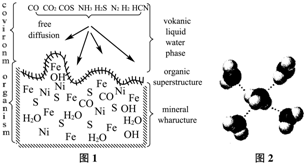
| 电离能/kJ?mol-1 | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 20.9 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |
第Ⅰ卷 (选择题 共21题,126分)
一、选择题(本题共6小题,每小题4分,共24分)
题号
1
2
3
4
5
6
7
8
9
答案
D
C
A
B
C
D
A
A
D
题号
10
11
12
13
14
15
16
17
答案
B
C
D
C
D
A
C
A
二、选择题
题号
18
19
20
21
答案
AD
BCD
B
BD
第Ⅱ卷(非选择题 共10题 共174分)
②45.85~45.95 (没有估读不给分)(3分)
③
④D或R1 (3分)
⑤实验电路图如右图(A表与R1连接对得3分,G表与R3连接对得3分)
(2)沿斜面上升时间t=v0/a=1.5s (2分)
所以总时间t总 =t+t′=4.5s (1分)
24.解:
⑵设轨道半径为r,A到D过程机械能守恒:
由以上三式得:
由图象纵截距得:6mg=12 得m=0.2kg (2分)
由L=0.5m时 △F=17N (1分)
代入得:
r=0.4m (2分)
25.解: (1)带电粒子在磁场中做圆周运动,有
(2)带电粒子在磁场中做圆周运动
26. (14分)
(1)共价键(或极性键)、离子键(各1分,共2分),Na、Al、Cl、H(漏写其中一个、元素符号错写或顺序写倒均扣2分)
.files/image175.gif) (2)Fe3++3H2O
(2)Fe3++3H2O .files/image176.gif) Fe(OH)3+3H+(未用可逆符号、未配平、Fe(OH)3标出沉淀符号各扣1分,不出现负分,共2分)
Fe(OH)3+3H+(未用可逆符号、未配平、Fe(OH)3标出沉淀符号各扣1分,不出现负分,共2分)
(3)Fe+4H2O ===== Fe3O4+4H2(未配平、未写条件各扣1分,化学式错误全错,共2分)
(4)c(OH_)+c(Cl_)=c(H+) (3分)
(5)30%(或0.3) (3分)
27.(14分)(1)C (2分)
(2)H2(g)+.files/image178.gif) O2(g)=H2O(l) △H= - 286kJ?mol―1(2分)(其它合理答案均给分)
O2(g)=H2O(l) △H= - 286kJ?mol―1(2分)(其它合理答案均给分)
(3)H2(2分)
(4)①2H2O+O2+4e- = 4OH-(2分);②1 (3分)
(5)y=x (3分)
28.(15分)
(1)温度(2分); (2))趁热过滤(2分)(漏写趁热两字扣1分,写成热过滤不扣分)
(3)取少量粗产品溶于适量的水中配成溶液,用洁净的铂丝(或铁丝)蘸取少量该溶液,放在火焰上灼烧,若火焰呈黄色,则表明该产品中含有一定量的杂质(或NaCl),反之,则没有。(3分)
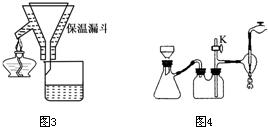
(4)布氏漏斗(1分);防止发生倒吸(2分);慢慢打开活塞d,然后关闭水龙头(2分)。
(5)将粗产品与水按质量比2:1混合(或将粗产品溶于适量的水),配成溶液,加热、搅拌,待晶体全部溶解后停止加热,冷却至室温后抽滤,然后用冰水(或95%的酒精)洗涤,抽滤,则得较高纯度的KNO3晶体。(3分)
29. (15分)
(1)消去反应、加成反应(还原反应)、酯化反应(每空1分,共3分)
(2)C6H10O4 (2分)
.files/image179.gif) |
(3) (3分)
.files/image180.gif)
.files/image181.gif)
.files/image182.gif) (4)
(4)
.files/image183.gif) |
|||||
.files/image184.gif) |
|||||
.files/image185.gif) |
|||||
(3分)(化学式有错误或漏写的不给分,条件未写扣1分)(另有合理答案给分)
.files/image186.gif)
.files/image187.gif) (5)
(5)
(每空2分,共4分)
30.I(14分,每格两分)
(1)杀死种子表面的微生物,防止微生物的呼吸作用干扰实验结果(只答其中一点就给分)
(2)种子呼吸作用吸收氧气的量大于二氧化碳的释放量,导致试管内气压下降
(3)8 (4)小于 (5)增大CO2的吸收面积
(6)避免幼苗因光合作用而干扰呼吸作用的气体量的变化
(7)10g被煮熟的发芽种子和等量的蒸馏水(全对给2分)
II( 14分)
(1)
②对实验组小鼠注射适量0.03%氯丙嗪,对照组小鼠注射等量的生理盐水;(2分)
(2)2、4、6 (1分)小鼠下丘脑体温调节中枢正常,能调节体温恒定;(1分)
1、5 (1分)氯丙嗪能抑制下丘脑体温调节中枢,使机体体温随环境温度的下降而下降(1分)
3 (1分)氯丙嗪能抑制下丘脑体温调节中枢,使机体体温随环境温度的升高而升高(1分)
(3)课题名称:探究氯丙嗪的浓度与体温调节的关系 (2分)(其他合理的也给分)
自变量操作:给实验组注射等量配制好具有一系列浓度梯度的氯丙嗪溶液 (2分)
因变量操作:用电子体温计分别测量两组小鼠的体温(2分))
31.(16分)
(1)XrXr 在减数分裂形成卵细胞过程中,少数的初级卵母细胞中的两条X染色体不分离,产生含XrXr的卵细胞或不含X染色体的卵细胞(2分),它们分别与XRY产生的正常精子结合(1分),产生了基因型为XrXrY、XR的果蝇,其表现型分别为白眼♀、红眼♂(1分)。
(2)(红眼)雄(1分) (白眼) 雌(1分) 红眼♀ 白眼♂ 白眼♀(全部正确给2分)
(3)XRXr 和 XRXrY (2分) XrY 和XrYY(2分)
(4)(4分,亲代基因型、表现型、子代基因型、表现型各1分,遗传符号不全的扣1分)
.files/image188.gif) |
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com