
题目列表(包括答案和解析)
氨是重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国化学家哈伯在1905年发明的,其合成原理为:N2(g) + 3H2(g)![]() 2NH3(g);
2NH3(g);
△H=―92.4 kJ/mol,他因此获得了1918年度诺贝尔化学奖。试回答下列问题:
⑴ 下列方法不适合实验室制取氨气的是 (填序号)。
A.向生石灰中滴入浓氨水 B.加热浓氨水
C.直接用氢气和氮气合成 D.向饱和氯化铵溶液中滴入浓氢氧化钠溶液
⑵ 合成氨工业中采取的下列措施可用勒夏特列原理解释的是 (填序号)。
A.采用较高压强(20 M Pa~50 M Pa)
B.采用500℃的高温
C.用铁触媒作催化剂
D.将生成的氨液化并及时从体系中分离出来,未反应的N2和H2循环到合成塔中
(3) 用数字化信息系统DIS(如下图Ⅰ所示:它由传感器、数据采集器和计算机组成)可以测定上述氨水的浓度。用酸式滴定管准确量取0.5000 mol/L醋酸溶液25.00 mL于烧杯中,以该种氨水进行滴定,计算机屏幕上显示出溶液导电能力随氨水体积变化的曲线如下图Ⅱ所示。


图Ⅰ 图Ⅱ
① 用滴定管盛氨水前,滴定管要用 润洗2~3遍,
② 试计算该种氨水的浓度: 。
③ 下列情况下,会导致实验结果c(NH3·H2O)偏低的是 。
A.滴定结束时仰视读数
B.量取25.00 mL醋酸溶液时,未用所盛溶液润洗滴定管
C.滴定时,因不慎将氨水滴在烧杯外
(4) 1998年希腊亚里士多德大学的Marnellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨。其实验装置如下图。

正极的电极反应式为: 。
氨是最重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g)![]() 2NH3(g);△H= ―92.4kJ/mol他因此获得了1918年诺贝尔化学奖。试回答下列问题:
2NH3(g);△H= ―92.4kJ/mol他因此获得了1918年诺贝尔化学奖。试回答下列问题:
(1)合成氨工业中采取的下列措施可用勒夏特列原理解释的是 (填序号)
A、采用较高压强(20Mpa~50Mpa)
B、采用500℃的高温
C、用铁触媒作催化剂
D、将生成的氨液化并及时从体系中分离出来,N2和H2循环到合成塔中并补充N2和H2
(2)下图是实验室模拟工业法合成氨的简易装置。简述检验有氨气生成的方法 。
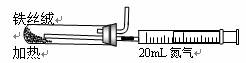
(3)在298K时,将10molN2和30molH2放入合成塔中,为何放出的热量小于924kJ? 。
(4)1998年希腊亚里斯多德大学的Marmellos和Stoukides采用高质子导电性的SCY陶瓷(能传递H+),实现了高温常压下高转化率的电化学合成氨。其实验装置如图。阴极的电极反应式 。

石墨和金刚石在一定条件下可相互转化:石墨 金刚石-Q.20世纪50年代,美国通用汽车公司在实验室利用高温、高压(2000℃,2×109Pa)将石墨转化成金刚石之后,1989年,日本科学家用炸药和碳粉“炸出”金刚石的消息引起人们的广泛关注.他们将炸药和碳粉混合并用石蜡固定后装入铝制敞口容器,沉入一个直径8m深约5m的混凝土水槽内,点火起爆,最后容器里可获得直径为0.002~0.003μm的超细金刚石粉.
金刚石-Q.20世纪50年代,美国通用汽车公司在实验室利用高温、高压(2000℃,2×109Pa)将石墨转化成金刚石之后,1989年,日本科学家用炸药和碳粉“炸出”金刚石的消息引起人们的广泛关注.他们将炸药和碳粉混合并用石蜡固定后装入铝制敞口容器,沉入一个直径8m深约5m的混凝土水槽内,点火起爆,最后容器里可获得直径为0.002~0.003μm的超细金刚石粉.
(1)从勒夏特列原理分析,上述两种制取金刚石的方法之所以能获得成功的原因是
[ ]
A.金刚石比石墨熔点低
B.金刚石的密度大于石墨
C.金刚石硬度很大
D.合成金刚石是吸热反应
(2)炸药爆炸的瞬间,可以产生4×1010Pa的超高压和5000℃的超高温,完全能达到石墨转化成金刚石的条件,你认为将炸药放在水槽内的最主要原因是
[ ]
(3)你认为工业上这种超细金刚石粉可以做
[ ]
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com