
题目列表(包括答案和解析)
为改善大气质量,国家拟于“十二五”期间,力争将CO2变为燃料或有机化学产品的构想变为现实,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.
Ⅰ.一种将CO2变为燃料或有机化学产品的构想分成3个步骤:
①利用浓碳酸钾溶液吸收空气中的CO2;
②将第①步吸收液电解产生H2和O2,同时分离出CO2;
③将第②步产生的H2(g)和CO2(g)在一定条件下转化成CH4(g)和H2O(l).
已知:H2(g)+![]() O2(g)=H2O(l) ΔH1=-285.8 kJ/mol
O2(g)=H2O(l) ΔH1=-285.8 kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH2=-889.6 kJ/mol
写出第③步反应的热化学方程式为________.
Ⅱ.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx.写出甲烷直接将NO2还原得到无污染的产物的化学方程式________.
(2)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)该反应的化学平衡常数表达式为K=________.
在一定温度下,将2 mol NO、1 mol CO充入1 L固定容积的容器中,反应过程中各物质的浓度变化如下图所示.
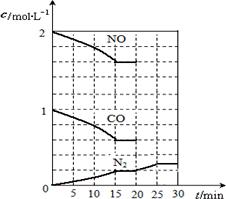
若保持温度不变,20 min时再向容器中充入CO、N2各0.6 mol,平衡将________移动(填“向左”、“向右”或“不”).
若20 min时改变反应条件,导致N2浓度发生如上图所示的变化,则改变的条件可能是________(填序号).
①加入催化剂
②降低温度
③缩小容器体积
④增加CO2的量
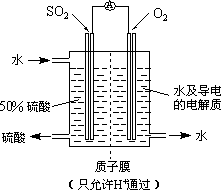
(3)最近,某科研单位研制成功一种处理SO2的方法:利用电化学原理将发电厂产生的大量SO2制成硫酸,装置如图,其电池反应方程式为:2SO2+O2+2H2O=2H2SO4,该电池电动势为1.06 V.实际过程中,将SO2通入电池的________极(填“正”或“负”),负极反应式为________.用这种方法处理SO2废气的优点是可回收大量有效能,副产品为H2SO4,减少环境污染.
| 1 |
| 2 |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
| c(N2)c2(CO2) |
| c2(NO)c2(CO) |
(14分)熔融盐燃料电池具有高的发电效率,因而受到重视。某燃料电池以熔融的![]() ,(其中不含
,(其中不含![]() 和
和![]() )为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电极反应式为:
)为电解质,以丁烷为燃料,以空气为氧化剂,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池负极电极反应式为:![]() 。试回答下列问题:
。试回答下列问题:
(1)该燃料电池的化学反应方程式为 ;
(2)正极电极反应式为 ;
(3)为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此,必须在通入的空气中加入一种物质,加入的物质是 ,它来自 ;
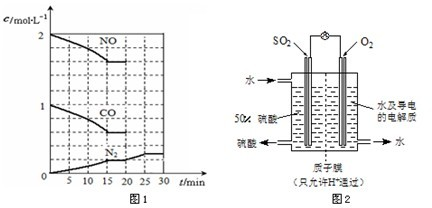
 (4)某学生想用该燃料电池和右图所示装置来电解饱和食盐水。
(4)某学生想用该燃料电池和右图所示装置来电解饱和食盐水。
①写出反应的离子方程式 。
②将湿润的淀粉![]() 试纸放在该装置附近,发现试纸变蓝,
试纸放在该装置附近,发现试纸变蓝,
待一段时间后又发现蓝色褪去,这是因为过量的![]() 将生成的
将生成的![]()
氧化。若反应的![]() 和
和![]() 的物质的量之比为5:l,且生成两种
的物质的量之比为5:l,且生成两种
酸。该反应的化学方程式为 ;
③若电解后得到![]()
![]()
![]() 溶液,则消耗
溶液,则消耗![]() 的体积在标准状况下为
的体积在标准状况下为 ![]() 。
。
 氢气是中学化学中常见的气体之一,它是一中新型的绿色能源,又是一种重要的化工原料.
氢气是中学化学中常见的气体之一,它是一中新型的绿色能源,又是一种重要的化工原料.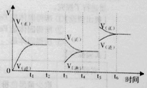
(15分)科学家认为,氢气是一种高效而无污染的理想能源,近20年来,对以氢气作为未来的动力燃料氢能源的研究获得了迅速发展。
(1)为了有效发展民用氢能源,首先必须制得廉价的氢气,下列可供开发又较经济且资源可持续利用的制氢气的方法是 。(选填字母)
| A.电解水 | B.锌和稀硫酸反应 |
| C.光解海水 | D.分解天然气 |

 CH3OH(g);ΔH =-90.8 kJ·mol-1
CH3OH(g);ΔH =-90.8 kJ·mol-1 CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1 CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1
CO2(g) + H2(g);ΔH=-41.3 kJ·mol-1 CH3OCH3(g) + CO2 (g)的ΔH=
CH3OCH3(g) + CO2 (g)的ΔH= 
一、选择题(本题包括
1.D 2.C 3.C 4.D 5.C 6.C 7.D 8.D 9.C l0.C
l1.B 12.C 13.C 14.C 15.D 16.C l 7.B l 8.D 19.B 20.A
二、本题包括1小题,共12分。
21.(12分)
(1)B中装无水硫酸铜,检验水蒸气;C中装澄清的石灰水,检验二氧化碳;(每空1分)
(2)验纯后点燃E处的气体,火焰呈蓝色。(2分,不答“验纯”扣1分)
(3)点燃前应验纯;CO有毒,实验要通风;加热时要均匀受热等。(2分)
(4)挥发出来的草酸蒸气与石灰水反应生成了草酸钙沉淀,会干扰CO2的检验(2分)
在装置B和C装置间增加一个装有水(或烧碱溶液)的洗气装置(2分)
三、本题包括3小题,共38分。
22.(每空2分,共12分)
(2)>
(3)A1 +3NH3?H2O=Al(OH)3↓ +3NH
+3NH3?H2O=Al(OH)3↓ +3NH
(4)NH4Al(SO4)2
(5)336
23.(每空2分,共l 2分)
(1)A:Si B:Mg
(2)抑制氯化镁水解
(3)①Si+2NaOH+H2O=Na2SiO3+2H2↑
③ Mg2Si+4HCl=SiH4↑+2MgCl2
24.(每空2分,共14分)
(1)
(2)O2+2CO2+4e =2CO
=2CO
(3)CO2 负极反应产物
②
③ 560
四、本题包括l小题,共l0分。
25.(1)Fe+H2SO4=FeSO4+H2↑(2分)
FeSO4+(NH4)2SO4+6H2O=(NH4)2Fe(SO4)2?6H2O(2分)
(2)解:设生成(NH4)2Fe(SO4)2?6H2O的物质的量为x mol。由上述方程式知:
H2SO4~FeSO4~(NH4)2Fe(SO4)2?6H2 O
1 mol l mol
15×3×10 mol x
mol
mol x
mol
x=0.045
生成(NH4)2Fe(SO4)2?6H2O的质量为:0.045 mol×
(3)① 5、1、8、1、5、4 H2O(2分)
② 83.33%。(2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com