
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
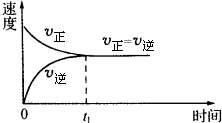
ªØ—ß∆Ω∫‚◊¥Ã¨ «÷∏‘⁄“ª∂®Ãıº˛œ¬µƒø…ƒÊ∑¥”¶£¨________µƒÀŸ¬ œýµ»£¨∑¥”¶ªÏ∫œŒÔ÷–∏˜◊È∑÷________µƒ◊¥Ã¨£Æ∆Ω∫‚◊¥Ã¨µƒΩ®¡¢»Áœ¬Õº 棨∑¥”¶ø™ º ±£¨“ÚŒ™________Ωœ¥Û£¨________Œ™0£¨À˘“‘________Ωœ¥Û£¨________Œ™0£ª∑¥”¶Ω¯–– ±£¨“ÚŒ™________≤ª∂œºı–°£¨À˘“‘________≤ª∂œºı–°£¨________≤ª∂œ‘ˆ¥Û£¨________≤ª∂œ‘ˆ¥Û£¨¥ÔµΩ’˝∑¥”¶ÀŸ¬ ”΃Ê∑¥”¶ÀŸ¬ œýµ» ±£¨∑¥”¶ÃÂœµæÕ¥ÔµΩ________£Æ(»Áœ¬ÕºÀ˘ æ)
ªØ—ß∑¥”¶‘≠¿Ì‘⁄ø∆—–∫Õ…˙≤˙÷–”–π„∑∫”¶”√°£
¢Ò°¢»ÁÕº◊∞÷√À˘ 棨A°¢B÷–µƒµÁº´Œ™∂ýø◊µƒ∂Ë–‘µÁº´£ªC°¢DŒ™º–‘⁄Ω˛”–Na2SO4»Ð“∫µƒ¬À÷ΩÃı…œµƒ≤¨º–£ªµÁ‘¥”–a°¢b¡Ωº´°£»ÙA°¢B÷–≥‰¬˙KOH»Ð“∫∫Ûµπ¡¢”⁄KOH»Ð“∫µƒÀÆ≤€÷–°£«–∂œK1£¨±’∫œK2°¢K3Õ®÷±¡˜µÁ°£

ªÿ¥œ¬¡–Œ £∫
£®1£© a «µÁ‘¥µƒ º´£¨–¥≥ˆA÷–µƒµÁº´∑¥”¶ ΩŒ™_____°£
£®2£© ™µƒNa2SO4¬À÷ΩÃı…œƒÐπ€≤ÏµΩµƒœ÷œÛ”–____________°£
£®3£©µÁΩ‚“ª∂Œ ±º‰∫Û£¨A°¢B÷–æ˘”–∆¯ÃÂ∞¸ŒßµÁº´£¨»Ù¥À ±«–∂œK2°¢K3£¨±’∫œK1£¨∑¢œ÷µÁ¡˜±Ìµƒ÷∏’Γ∆∂Ø£¨–¥≥ˆ¥À ±B÷–µƒµÁº´∑¥”¶ ΩŒ™ °£
¢Ú°¢º◊¥º «“ª÷÷ø…‘Ÿ…˙ƒÐ‘¥£¨æþ”–π„∑∫µƒø™∑¢∫Õ”¶”√«∞æ∞°£π§“µ…œ“ª∞„≤…”√œ¬¡–∑¥”¶∫œ≥…º◊¥º£∫CO(g)£´2H2(g)
 CH3OH(g)
¶§H£¨œ¬±ÌÀ˘¡– ˝æð «∏√∑¥”¶‘⁄≤ªÕ¨Œ¬∂»œ¬µƒªØ—ß∆Ω∫‚≥£ ˝(K)°£«Îªÿ¥œ¬¡–Œ £∫
CH3OH(g)
¶§H£¨œ¬±ÌÀ˘¡– ˝æð «∏√∑¥”¶‘⁄≤ªÕ¨Œ¬∂»œ¬µƒªØ—ß∆Ω∫‚≥£ ˝(K)°£«Îªÿ¥œ¬¡–Œ £∫
|
Œ¬∂» |
250°Ê |
300°Ê |
350°Ê |
|
K |
2.041 |
0.270 |
0.012 |
£®4£©”…±Ì÷– ˝æð≈–∂œ¶§H 0£®ÃÓ°∞£æ°±°¢°∞£º°±ªÚ°∞£Ω°±£©°£
£®5£©∆‰À˚Ãıº˛≤ª±‰£¨÷ª∏ƒ±‰∆‰÷–“ª∏ˆÃıº˛£¨œ¬¡–¥Î ©ø…÷∏þº◊¥º≤˙¬ µƒ « °£
A£Æ…˝∏þŒ¬∂»£ªB£Æ π”√∫œ µƒ¥þªØº¡£ªC£ÆÀı–°»ð∆˜µƒ»ðª˝£ªD£Æ≥‰»Îπ˝¡øµƒH2£ªE£Æ∫„—π ±£¨≥‰»ÎHe£ªF£Æ¥”ÃÂœµ÷–∑÷¿Î≥ˆCH3OH
£®6£©ƒ≥Œ¬∂»œ¬£¨Ω´2mol CO∫Õ6 mol H2≥‰»Î2L√б’»ð∆˜÷–£¨∑¥”¶Ω¯––µΩ4minƒ©¥ÔµΩ∆Ω∫‚£¨¥À ±≤‚µ√c(CO) £Ω0.2 mol/L £¨‘Ú0~4minƒ⁄H2µƒ∑¥”¶ÀŸ¬ Œ™ £ª»Ù±£≥÷Œ¬∂»»ðª˝≤ª±‰‘ŸœÚ∆‰÷–≥‰»Î“ª∂®¡øµƒCH3OH£¨÷ÿ–¬¥ÔµΩªØ—ß∆Ω∫‚◊¥Ã¨£¨”Α≠∆Ω∫‚◊¥Ã¨œý±»£¨¥À ±∆Ω∫‚ªÏ∫œ∆¯ÃÂ÷–CH3OHµƒÃª˝∑÷ ˝ £®ÃÓ°∞±‰¥Û°±°¢°∞±‰–°°±°¢ªÚ°∞≤ª±‰°±£©°£
ªØ—ß∑¥”¶‘≠¿Ì‘⁄ø∆—–∫Õ…˙≤˙÷–”–π„∑∫”¶”√°£
¢Ò°¢»ÁÕº◊∞÷√À˘ 棨A°¢B÷–µƒµÁº´Œ™∂ýø◊µƒ∂Ë–‘µÁº´£ªC°¢DŒ™º–‘⁄Ω˛”–Na2SO4»Ð“∫µƒ¬À÷ΩÃı…œµƒ≤¨º–£ªµÁ‘¥”–a°¢b¡Ωº´°£»ÙA°¢B÷–≥‰¬˙KOH»Ð“∫∫Ûµπ¡¢”⁄KOH»Ð“∫µƒÀÆ≤€÷–°£«–∂œK1£¨±’∫œK2°¢K3Õ®÷±¡˜µÁ°£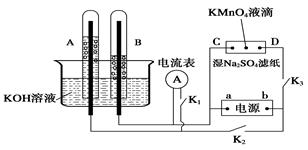
ªÿ¥œ¬¡–Œ £∫
£®1£© a «µÁ‘¥µƒ º´£¨–¥≥ˆA÷–µƒµÁº´∑¥”¶ ΩŒ™_____°£
£®2£© ™µƒNa2SO4¬À÷ΩÃı…œƒÐπ€≤ÏµΩµƒœ÷œÛ”–____________°£
£®3£©µÁΩ‚“ª∂Œ ±º‰∫Û£¨A°¢B÷–æ˘”–∆¯ÃÂ∞¸ŒßµÁº´£¨»Ù¥À ±«–∂œK2°¢K3£¨±’∫œK1£¨∑¢œ÷µÁ¡˜±Ìµƒ÷∏’Γ∆∂Ø£¨–¥≥ˆ¥À ±B÷–µƒµÁº´∑¥”¶ ΩŒ™ °£
¢Ú°¢º◊¥º «“ª÷÷ø…‘Ÿ…˙ƒÐ‘¥£¨æþ”–π„∑∫µƒø™∑¢∫Õ”¶”√«∞æ∞°£π§“µ…œ“ª∞„≤…”√œ¬¡–∑¥”¶∫œ≥…º◊¥º£∫CO(g)£´2H2(g)  CH3OH(g) ¶§H£¨œ¬±ÌÀ˘¡– ˝æð «∏√∑¥”¶‘⁄≤ªÕ¨Œ¬∂»œ¬µƒªØ—ß∆Ω∫‚≥£ ˝(K)°£«Îªÿ¥œ¬¡–Œ £∫
CH3OH(g) ¶§H£¨œ¬±ÌÀ˘¡– ˝æð «∏√∑¥”¶‘⁄≤ªÕ¨Œ¬∂»œ¬µƒªØ—ß∆Ω∫‚≥£ ˝(K)°£«Îªÿ¥œ¬¡–Œ £∫
| Œ¬∂» | 250°Ê | 300°Ê | 350°Ê |
| K | 2.041 | 0.270 | 0.012 |
œ¬¡–Àµ∑®’˝»∑µƒ «
A£Æø…ƒÊ∑¥”¶µƒªØ—ß∑¥”¶ÀŸ¬ «÷∏’˝∑¥”¶ÀŸ¬
B£Æ‘⁄ø…ƒÊ∑¥”¶¿Ô’˝∑¥”¶µƒÀŸ¬ «’˝÷µ£¨ƒÊ∑¥”¶µƒÀŸ¬ «∏∫÷µ
C£Æ‘⁄“ª∂®Ãıº˛œ¬£¨µ±ø…ƒÊ∑¥”¶µƒ’˝∑¥”¶ÀŸ¬ ”΃Ê∑¥”¶ÀŸ¬ œýµ» ±£¨∑¥”¶ŒÔ∫Õ…˙≥…ŒÔµƒ≈®∂»≤ª‘Ÿ∑¢…˙±‰ªØ£¨’‚æÕ «∏√∑¥”¶À˘¥ÔµΩµƒœÞ∂»
D£Æ∂‘”⁄ø…ƒÊ∑¥”¶¿¥Àµ£¨∑¥”¶ŒÔ◊™ªØŒ™…˙≥…ŒÔ√ª”–“ª∂®µƒœÞ∂»
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com