
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
|
‘⁄101 kPa∫Õ25°Ê ±£¨”–∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã Ω£∫H2(g)£´1/2O2(g)£ΩH2O(g)£ª °˜H£Ω£≠241.8 kJ/mol£¨H2(g)£´1/2O2(g)£ΩH2O(1)£ª°˜H£Ω£≠285.8 kJ/mol£Æœ¬¡–Àµ∑®÷–¥ÌŒÛµƒ « | |
| [°°°°] | |
A£Æ |
H2»º…’…˙≥…1 mol H2O(g) ±£¨∑≈≥ˆ241.8 kJµƒ»»¡ø |
B£Æ |
H2µƒ»º…’»»Œ™285.8 kJ |
C£Æ |
O2«∞√ʵƒ1/2±Ì æ≤Œº”∑¥”¶µƒO2µƒŒÔ÷ µƒ¡ø |
D£Æ |
1 mol ¡˜Ã¨ÀƱ‰≥…ÀÆ’Ù∆¯ ±Œ¸ ’44 kJµƒ»»¡ø |
|
‘⁄101 kPa∫Õ25°Ê ±£¨”–∑¥”¶µƒ»»ªØ—ß∑Ω≥Ã Ω£∫H2(g)£´1/2O2(g)£ΩH2O(g)£ª¶§H£Ω£≠241.8 kJ/mol£¨H2(g)£´1/2O2(g)£ΩH2O(1)£ª¶§H£Ω£≠285.8 kJ/mol£Æœ¬¡–Àµ∑®÷–¥ÌŒÛµƒ «£∫ | |
| [°°°°] | |
A£Æ |
H2»º…’…˙≥…1 mol°°H2O(g) ±£¨∑≈≥ˆ241.8 kJµƒ»»¡ø |
B£Æ |
H2µƒ»º…’»»Œ™285.8 kJ |
C£Æ |
O2«∞√ʵƒ1/2±Ì æ≤Œº”∑¥”¶µƒO2µƒŒÔ÷ µƒ¡ø |
D£Æ |
1 mol“∫èÀƱ‰≥…ÀÆ’Ù∆¯ ±Œ¸ ’44 kJµƒ»»¡ø |
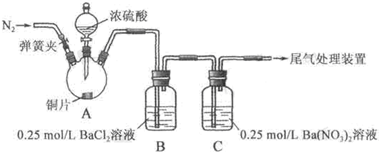
| ≤Ÿ◊˜ | œ÷œÛ |
| πÿ±’µØª…º–£¨µŒº”“ª∂®¡ø≈®¡ÚÀ·£¨º”»» | A÷–”–∞◊ŒÌ…˙≥…£¨Õ≠∆¨±Ì√Ê≤˙…˙∆¯≈ð B÷–”–∆¯≈ð√∞≥ˆ£¨≤˙…˙¥Û¡ø∞◊…´≥¡µÌ C÷–≤˙…˙∞◊…´≥¡µÌ£¨“∫√Ê…œ∑Ω¬‘œ‘«≥◊ÿ…´≤¢÷Ω•œ˚ ß |
| ¥Úø™µØª…º–£¨Õ®»ÎN2£¨Õ£÷πº”»»£¨“ª∂Œ ±º‰∫Ûπÿ±’ | --- |
| ¥”B°¢C÷–∑÷±»°…Ÿ¡ø∞◊…´≥¡µÌ£¨º”œ°—ŒÀ· | æ˘Œ¥∑¢œ÷∞◊…´≥¡µÌ»ÐΩ‚ |
| ||
| ||
| º◊ | ¥Û¡ø∞◊…´≥¡µÌ |
| ““ | …Ÿ¡ø∞◊…´≥¡µÌ |
‘⁄101kPa∫Õ25°Ê ±£¨»»ªØ—ß∑Ω≥Ã Ω£∫H2(g) + 1/2O2(g) =H2O(g)£ª°˜H=-241.8kJ/mol£¨H2(g) + 1/2O2(g) =H2O(1)£ª°˜H=-285.8kJ/mol°£œ¬¡–Àµ∑®÷–¥ÌŒÛµƒ «£∫ ( )
A£ÆH2»º…’…˙≥…1molH2O(g) ±£¨∑≈≥ˆ241.8kJµƒ»»¡ø
B£ÆH2µƒ»º…’»»Œ™285.8kJ
C£ÆO2 «∞√ʵƒ1/2±Ì æ≤Œº”∑¥”¶µƒO2µƒŒÔ÷ µƒ¡ø
D£Æ1mol“∫èÀƱ‰≥…ÀÆ’Ù∆¯ ±Œ¸ ’44kJµƒ»»¡ø
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com