
题目列表(包括答案和解析)
| 操作 | 实验现象及结论 | |
| 方案1 | 取少量黄色溶液,加入NaOH | 最终生成红褐色沉淀,说明溴水和FeSO4溶液发生了化学反应 |
| 方案2 | 取少量黄色溶液,加入淀粉碘化钾溶液 | 溶液变蓝色,说明未发生化学反应 |
| 方案3 | 取少量黄色溶液,加入四氯化碳,振荡 | 下层溶液呈橙红色,说明未发生化学反应 |
: 关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一:“理论派”认为电解氯化铜溶液后溶液的pH升高。观点二:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH值的变化如右图曲线关系。请回答下列问题:
关于“电解氯化铜溶液时的pH变化”问题,化学界有以下两种不同的观点:观点一:“理论派”认为电解氯化铜溶液后溶液的pH升高。观点二:“实验派”经过反复、多次、精确的实验测定,证明电解氯化铜溶液时pH值的变化如右图曲线关系。请回答下列问题:
①电解前氯化铜溶液的pH值处于A点位置的原因是: (用离子方程式说明)。
②“理论派”所持观点的理论依据是: 。
③“实验派”的实验结论是 ,他们所述“精确实验”是通过
确定的。
④你持何种观点?你所持观点的理由是(从化学原理加以简述) 。
方法:本题要从电解过程中的实际情况加以分析,即阳极产生的Cl2不能全部析出,而有部分溶于阳极区的溶液中,以此造成溶液的pH下降。
![]() 分析:①中电解前氯化铜溶液的pH值处于A点位置,显酸性,显然,其酸性的原因是CuCl2水解之故;②中“理论派”所持观点的是从电解过程中物质随着电解的进行,CuCl2溶液的浓度下降,造成Cu2+水解产生的H+浓度下降。③中实验派的实验结论可从图示找得答案,随电解的进行,酸性增强。④回答个人所持观点,应尊重实验事实,从实验的实际情况出发,以此可得解题结果。
分析:①中电解前氯化铜溶液的pH值处于A点位置,显酸性,显然,其酸性的原因是CuCl2水解之故;②中“理论派”所持观点的是从电解过程中物质随着电解的进行,CuCl2溶液的浓度下降,造成Cu2+水解产生的H+浓度下降。③中实验派的实验结论可从图示找得答案,随电解的进行,酸性增强。④回答个人所持观点,应尊重实验事实,从实验的实际情况出发,以此可得解题结果。
(10分)今有一金属卤化物A,在水溶液中完全电离,生成一种阴离子和一种阳离子,个数比为4∶1。取4.004g A溶于水,加入过量AgNO3溶液,生成2.294g白色沉淀。经测定,阳离子由X和Y两种元素构成,结构呈正方体状,十分对称。任意两个相离最远的X原子的连线为此离子的三重轴,任意两个相离最远的Y原子的连线为此离子的四重轴(n重轴表示某物质绕此轴旋转360°/n的角度,不能察觉其是否旋转过)。
6-1 写出A的化学式 (阴阳离子分开写)
6-2 写出X和Y的元素符号 、
6-3 在右框中画出A溶液中阳离子的结构:
6-4 小明把一种常见含X的二元化合物的晶胞去掉所有的X原子,发现剩余部分与A溶液中阳离子的结构竟十分相似。这种常见二元化合物是 。
6-5 你认为A溶液中阳离子中,同种原子间存在着什么样的作用力,并简略说明你的依据:
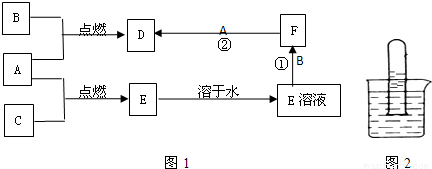
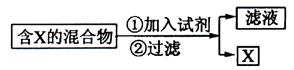
(Ⅰ)混合物的分离与提纯在化学实验中占有重要的位置。下图表示从固体混合物中分离X的方案,请回答有关问题。
![]() (1)
(1)
若按照以上图示从某金属粉末(含有Au、Ag和Cu)中分离Au,加入的试剂是 ,有关反应的化学方程式为 ;
![]() (2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作) 。
(2)为提纯某Fe2O3样品(主要杂质有SiO2、A12O3),请设计一种以框图形式表示的实验方案(注明物质和操作) 。
(Ⅱ)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。
(1)该工艺的中间过程会发生反应: ,反应的氧化剂是______________,氧化产物为__________
,反应的氧化剂是______________,氧化产物为__________
(2)在精炼铜的过程中,电解液中![]() 逐渐下降,
逐渐下降,![]() 、
、![]() 会逐渐增加,所以需定时除去其中的
会逐渐增加,所以需定时除去其中的![]() 、
、![]() 。下表为几种物质的溶度积。
。下表为几种物质的溶度积。
| 物质 |
|
|
|
|
| 溶度积 |
|
|
|
|
甲同学设计了如下除杂方案:
![]()
①试剂a是__________,其目的是____________________________________;根据溶度积该方案能够除去的杂质金属阳离子是____________。写出检验该杂质金属阳离子的操作方法:____________________________________________________________________________.
②乙同学在查阅资料时发现,“工业原料氯化铵中含杂质氯化铁,使其溶入水,再加入氨水
调节pH至7~8,可使![]() 生成
生成![]() 。沉淀而除去。”乙同学认为甲同学的方案中也
。沉淀而除去。”乙同学认为甲同学的方案中也
应该将溶液pH调至7~8。你认为乙同学的建议是否正确?________(填“是”或“否”),
理由是________________________________________________________________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com