
题目列表(包括答案和解析)
 FeO(s)+CO(g)的平衡常数为K1,反应②Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1,反应②Fe(s)+H2O(g) FeO(s)+H2(g)的平衡常数为K2。在不同温度下,K1、K2的值如下
FeO(s)+H2(g)的平衡常数为K2。在不同温度下,K1、K2的值如下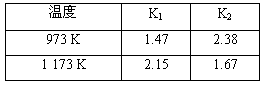
 CO(g)+H2O(g),写出该反应的平衡常数K3的数学表达式:K3=________。
CO(g)+H2O(g),写出该反应的平衡常数K3的数学表达式:K3=________。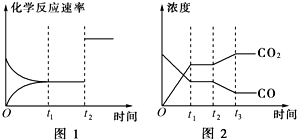
现有下列十种物质:①H2;②铝;③CaO;④CO2;⑤H2SO4;⑥Ba(OH)2;⑦红褐色的氢氧化铁液体;⑧氨水;⑨稀硝酸;⑩Al2(SO4)3
(1)按物质的分类方法填写表格的空白处:

(2)上述十种物质中有两种物质之间可发生离子反应:H++OH-![]() H2O,该离子反应对应的化学方程式为________.
H2O,该离子反应对应的化学方程式为________.
(3)⑩在水中的电离方程式为________,17.1 g⑩溶于水配成250 mL溶液,SO![]() 的粒子数为________,SO
的粒子数为________,SO![]() 的物质的量浓度为________.
的物质的量浓度为________.
(4)少量的④通入⑥的溶液中反应的离子方程式为________.
(5)②与⑨发生反应的化学方程式为:Al+4HNO3=Al(NO3)3+NO↑+2H2O,该反应的氧化剂是________(填化学式),还原剂与氧化剂的物质的量之比是________,当有5.4 g Al发生反应时,转移电子的物质的量为________.该反应的离子方程式为________.
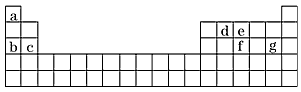
| |||||||||||||||||||||||||||||||||||
|
已知常温下,N2(g)和H2(g)生成2 mol NH3(g)放出92.4 kJ热量.现有甲、乙两个容积相同的密闭容器,在常温下:①向密闭容器甲中通入1 mol N2和3 mol H2,达到平衡时放出热量Q1 kJ.②向密闭容器乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2 kJ.则下列关系式正确的是 | |
| [ ] | |
A. |
92.4>Ql>2Q2 |
B. |
92.4=Q1<2Q2 |
C. |
Q1=2Q2=92.4 |
D. |
Q1=2Q2<92.4 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com