
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
¬»Μ·Ά≠ΨßΧε(CuCl2ΓΛxH2O) «÷Ί“ΣΒΡΜ·ΙΛ‘≠ΝœΘ§Ω…”ΟΉςΖ¥”ΠΒΡ¥ΏΜ·ΦΝΓΔœϊΕΨΦΝΒ»Θ°”ΟΩΉ»Η ·[÷ς“ΣΚ§Cu2(OH)2CO3Θ§ΜΙΚ§…ΌΝΩFeΓΔSiΒΡΜ·ΚœΈο]÷Τ±Η¬»Μ·Ά≠ΨßΧεΘ§ΖΫΑΗ»γœ¬ΘΚ
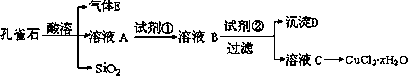
“―÷ΣΘΚΔώΘ°Cu(OH)2ΓΔCuOΩΣ ΦΖ÷ΫβΒΡΈ¬Ε»Ζ÷±πΈΣ80ΓφΚΆ900ΓφΘ°
ΔρΘ°”–ΙΊΫπ τάκΉ”¥”ΩΣ Φ≥ΝΒμΒΫ≥ΝΒμΆξ»Ϊ ±»ή“ΚΒΡpHΘΚ
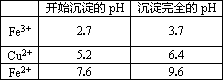
(1)»τ»ή“ΚAΚ§”–ΒΡΫπ τάκΉ””–Cu2+ΓΔFe2+ΓΔFe3+Θ§‘ρ ‘ΦΝΔΌΉνΚΟΈΣ________(ΧνΉ÷ΡΗ)Θ°
aΘ°(NH4)2S
bΘ°H2O2
cΘ°NaClO
dΘ°Cl2
(2)Φ” ‘ΦΝΔΎΒΡΡΩΒΡ «________Θ§”…»ή“ΚCΜώΒΟCuCl2ΓΛxH2OΘ§–η“ΣΨ≠ΙΐΦ”»»≈®ΥθΓΔ________ΓΔΙΐ¬ΥΒ»≤ΌΉςΘ°
(3)ΈΣΝΥ≤βΕ®÷ΤΒΟΒΡ¬»Μ·Ά≠ΨßΧε(CuCl2ΓΛxH2O)÷–x÷ΒΘ§”–»γœ¬ΝΫ÷÷ Β―ιΖΫΑΗΘΚ
ΖΫΑΗ“ΜΘΚ≥Τ»Γa gΨßΧεΉΤ…’÷Ν÷ ΝΩ≤Μ‘ΌΦθ«αΈΣ÷ΙΘ§ά以ΓΔ≥ΤΝΩΥυΒΟΈόΥ°CuCl2ΒΡ
÷ ΝΩΈΣb gΘ°
ΖΫΑΗΕΰΘΚ≥Τ»Γa gΨßΧεΓΔΦ”»κΉψΝΩ«β―θΜ·ΡΤ»ή“ΚΘ§Ιΐ¬ΥΓΔœ¥Β”ΓΔΦ”»»≥ΝΒμ(ΩΊ÷ΤΈ¬Ε»‘ΦΈΣ120Γφ)÷Ν÷ ΝΩ≤Μ‘ΌΦθ«αΈΣ÷ΙΘ§≥ΤΝΩΥυΒΟΙΧΧεΒΡ÷ ΝΩΈΣbgΘ°
‘ρ…œ ωΖΫΑΗ÷–≤ΜΚœάμΒΡ «________Θ§‘≠“ρ «________Θ°
“άΨίΚœάμΖΫΑΗΦΤΥψΒΟxΘΫ________(”ΟΚ§aΓΔbΒΡ¥ζ ΐ Ϋ±μ Ψ)Θ°

| ‘ΣΥΊ | A | B | C | D |
| ΫαΙΙ–‘÷ –≈œΔ |
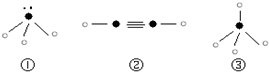
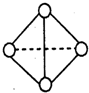
ΜυΧ§‘≠Ή”÷–ΒγΉ”’ΦΨί»ΐ÷÷ΡήΝΩ≤ΜΆ§ΒΡ‘≠Ή”ΙλΒάΘ§«“ΟΩ÷÷ΙλΒά÷–ΒΡΒγΉ” ΐœύΆ§ | ‘≠Ή”ΚΥΆβ”–ΝΫΗωΒγΉ”≤ψΘ§ΉνΆβ≤ψ”–3ΗωΈ¥≥…Ε‘ΒΡΒγΉ” | ΜυΧ§‘≠Ή”ΒΡM≤ψ”–2Ε‘≥…Ε‘ΒΡpΒγΉ” | Τδ‘≠Ή”–ρ ΐ±»AΓΔBΓΔC»ΐ÷÷‘ΣΥΊ‘≠Ή”ΒΡ÷ Ή” ΐΉήΚΆΜΙ…Ό1Θ§”–+1ΓΔ+2ΝΫ÷÷≥ΘΦϊΜ·ΚœΦέ |
| A-O | A=O | F-O | F=O | |
| ΦϋΡήΘ®KJ/molΘ© | 360 | 803 | 464 | 640 |
 Γ±±μ Ψ…œ ωœύΙΊ‘ΣΥΊΒΡ‘≠Ή”÷–≥ΐ»ΞΉνΆβ≤ψΒγΉ”ΒΡ Θ”ύ≤ΩΖ÷Θ§ΓΑ
Γ±±μ Ψ…œ ωœύΙΊ‘ΣΥΊΒΡ‘≠Ή”÷–≥ΐ»ΞΉνΆβ≤ψΒγΉ”ΒΡ Θ”ύ≤ΩΖ÷Θ§ΓΑ Γ±±μ Ψ«β‘≠Ή”Θ§–ΓΚΎΒψΓΑ
Γ±±μ Ψ«β‘≠Ή”Θ§–ΓΚΎΒψΓΑ Γ±±μ ΨΟΜ”––Έ≥…Ι≤ΦέΦϋΒΡΉνΆβ≤ψΒγΉ”Θ§ΕΧœΏ±μ ΨΙ≤ΦέΦϋΘ°
Γ±±μ ΨΟΜ”––Έ≥…Ι≤ΦέΦϋΒΡΉνΆβ≤ψΒγΉ”Θ§ΕΧœΏ±μ ΨΙ≤ΦέΦϋΘ°

| ‘ΣΥΊ | A | B | C | D |
| ΫαΙΙ–‘÷ –≈œΔ |
ΜυΧ§‘≠Ή”÷–ΒγΉ”’ΦΨί»ΐ÷÷ΡήΝΩ≤ΜΆ§ΒΡ‘≠Ή”ΙλΒάΘ§«“ΟΩ÷÷ΙλΒά÷–ΒΡΒγΉ” ΐœύΆ§ | ‘≠Ή”ΚΥΆβ”–ΝΫΗωΒγΉ”≤ψΘ§ΉνΆβ≤ψ”–3ΗωΈ¥≥…Ε‘ΒΡΒγΉ” | ΜυΧ§‘≠Ή”ΒΡM≤ψ”–2Ε‘≥…Ε‘ΒΡpΒγΉ” | Τδ‘≠Ή”–ρ ΐ±»AΓΔBΓΔC»ΐ÷÷‘ΣΥΊ‘≠Ή”ΒΡ÷ Ή” ΐΉήΚΆΜΙ…Ό1Θ§”–+1ΓΔ+2ΝΫ÷÷≥ΘΦϊΜ·ΚœΦέ |
| A-O | A=O | F-O | F=O | |
| ΦϋΡήΘ®KJ/molΘ© | 360 | 803 | 464 | 640 |



| ‘ΣΥΊ | A | B | C | D |
| ΫαΙΙ–‘÷ –≈œΔ | ΜυΧ§‘≠Ή”÷–ΒγΉ”’ΦΨί»ΐ÷÷ΡήΝΩ≤ΜΆ§ΒΡ‘≠Ή”ΙλΒάΘ§«“ΟΩ÷÷ΙλΒά÷–ΒΡΒγΉ” ΐœύΆ§ | ‘≠Ή”ΚΥΆβ”–ΝΫΗωΒγΉ”≤ψΘ§ΉνΆβ≤ψ”–3ΗωΈ¥≥…Ε‘ΒΡΒγΉ” | ΜυΧ§‘≠Ή”ΒΡM≤ψ”–2Ε‘≥…Ε‘ΒΡpΒγΉ” | Τδ‘≠Ή”–ρ ΐ±»AΓΔBΓΔC»ΐ÷÷‘ΣΥΊ‘≠Ή”ΒΡ÷ Ή” ΐΉήΚΆΜΙ…Ό1Θ§”–+1ΓΔ+2ΝΫ÷÷≥ΘΦϊΜ·ΚœΦέ |
| A-O | A=O | F-O | F=O | |
| ΦϋΡήΘ®KJ/molΘ© | 360 | 803 | 464 | 640 |
 Γ±±μ Ψ…œ ωœύΙΊ‘ΣΥΊΒΡ‘≠Ή”÷–≥ΐ»ΞΉνΆβ≤ψΒγΉ”ΒΡ Θ”ύ≤ΩΖ÷Θ§ΓΑ
Γ±±μ Ψ…œ ωœύΙΊ‘ΣΥΊΒΡ‘≠Ή”÷–≥ΐ»ΞΉνΆβ≤ψΒγΉ”ΒΡ Θ”ύ≤ΩΖ÷Θ§ΓΑ Γ±±μ Ψ«β‘≠Ή”Θ§–ΓΚΎΒψΓΑ
Γ±±μ Ψ«β‘≠Ή”Θ§–ΓΚΎΒψΓΑ Γ±±μ ΨΟΜ”––Έ≥…Ι≤ΦέΦϋΒΡΉνΆβ≤ψΒγΉ”Θ§ΕΧœΏ±μ ΨΙ≤ΦέΦϋΘ°
Γ±±μ ΨΟΜ”––Έ≥…Ι≤ΦέΦϋΒΡΉνΆβ≤ψΒγΉ”Θ§ΕΧœΏ±μ ΨΙ≤ΦέΦϋΘ°

ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com