
题目列表(包括答案和解析)

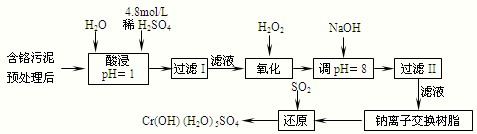
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cu2+ | Cr3+ |
| 开始沉淀时的pH | 1.9 | 7.0 | -- | -- | 4.7 | -- |
| 沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8 | 6.7 | 9 (>9溶解) |
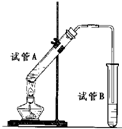
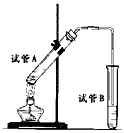
(13分)如图所示,中学化学实验室采用该装置用于制备乙酸乙酯。
⑴写出制备乙酸乙酯的化学方程式 ▲ 。
⑵浓硫酸在实验中的作用是 ▲ 、 ▲ 。
⑶加热一段时间后,在试管B饱和碳酸钠溶液的液面上方有一 层油层,在油、水交界处观察到有气泡产生,气泡的主要成分是 ▲ 。
⑷停止加热,取下试管B ,嗅闻管内液体气味,闻到更多的是刺激性气味,这是因为物质的挥发等因素导致产品混有杂质,如 ▲ 和 ▲ 等,为进一步验证产物中某些杂质存在,在保持试管B相对稳定情况下,沿试管内壁滴入紫色石蕊试液,静置片刻会在试管内油层下方明显看到液体呈现三种颜色,由上而下分别为红色、紫色、蓝色,其原因可能是 ▲ ,故产品需进行提纯。
⑸已知乙醇能和氯化钙结合。将所得产品依次用饱和碳酸钠溶液、饱和食盐水、饱和氯化钙溶液洗涤油层,分别分液。用饱和食盐水洗涤去除油层中可能含有的 ▲ 杂质,减少乙酸乙酯的溶解,并防止对下面操作产生不利影响。
⑹在上述操作后,在所得油状液体中加入无水硫酸钠充分振荡,倾倒出油状液体,再进行 ▲ (填提纯的操作方法),收集74~78℃的馏分即可获得较纯净的乙酸乙酯。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com