
题目列表(包括答案和解析)
| 1 |
| 2 |
| 3 |
| 2 |

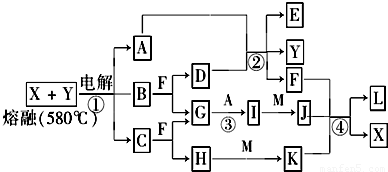
下图所示物质中,只有X是单质,常温下A和B呈气态,且B是导致酸雨的大气污染物,D是淡黄色固体.

据此回答下列问题:
(1)物质D的电子式为________,其阴阳离子个数比为________.
(2)请列举物质F的两种用途:________、________.
(3)写出X和Y反应的化学方程式________;A与D反应时若生成21.2 g的C,则反应中转移电子数目为________.
(4)请写出Y和F反应的离子方程式________.
下图所示物质中,只有X是单质,常温下A和B呈气态,且B是导致酸雨的大气污染物,D是淡黄色固体。

据此回答下列问题:
(1)元素X在元素周期表中位于 周期 族。
(2)物质D的电子式为 ,其阴阳离子个数比为 。
(3)请列举物质F的两种用途: 、 。
(4)写出X和Y反应的化学方程式 ;若生成的B在标准状况下的体积为22.4L,则反应中转移电子数目为 。
(5)请写出Y和F反应的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com